Classification and Selection of Deoxyribozymes and Its Applications
-
摘要: DNA核酶是通过指数富集配体的系统进化技术(Systematic Evolution of Ligands by Exponential Enrichment,SELEX)筛选出来的具有催化活性的DNA分子。本文重点综述了DNA核酶的分类、筛选及主要应用。根据其催化作用方式,可将DNA核酶分为切割类、连接类、磷酸化类和其他类,其中切割类和连接类占的比例较大。目前DNA核酶的底物主要还是以核酸居多。DNA核酶的筛选主要是采用生物素-链霉亲和素法和聚丙烯酰胺凝胶电泳法来分离有催化活性的DNA分子。目前DNA核酶在金属离子检测、基因治疗和DNA分子加密系统中都呈现出较好的应用前景。
-
关键词:
- DNA核酶 /
- 分类 /
- 筛选 /
- 指数富集的配体系统进化技术(SELEX)
Abstract: Deoxyribozyme is a kind of DNA molecule with catalytic activity. It can be selected by systematic evolution of ligands by exponential enrichment (SELEX). This review focuses on the classification, selection and main applications of deoxyribozymes. According to the catalysis, deoxyribozymes can be classified into cleaved, ligated, phosphorylated and other types. Nowadays the cleaved and ligated types account for a large proportion, and nucleic acids are the main substrates of deoxyribozymes. Biotin-streptavidin method or polyacrylamide gel electrophoresis is often used to separate the catalytic DNA in selection of deoxyribozymes. Deoxyribozymes have good application prospect in metal ion detection, gene therapy and DNA molecular encryption system. -
1982年Cech领导的团队首先发现四膜虫核糖体RNA具有自我催化功能[1],之后Altman实验室也进一步证明了RNA的催化功能[2]。这些具有催化功能的核酸被称为核酶。核酶的发现,打破了“酶就是蛋白质”的传统观念,大大促进了酶学的发展。目前发现的天然核酶都是RNA分子,为RNA核酶。1990年Joyce实验室等开发出了人造RNA核酶,进一步丰富了核酶的外延[3]。受RNA核酶的启发,科学家们将目光放在了DNA上面,试图寻找DNA核酶。然而,由于天然DNA的双链模式和双螺旋结构限制了双链DNA分子作为酶的潜力,所以目前天然双链DNA核酶尚未发现,而化学合成的单链DNA分子,由于不再受双链结构的限制,具有较高的自由度,成为DNA核酶的理想分子[4-5]。1994年Breaker和Joyce[6]利用SELEX技术筛选出一种以单链DNA为基础成分的核酶,它能在Pb2+的辅助下水解RNA特定位置的磷酸二酯键,成为首个报道的DNA核酶。
筛选DNA核酶所用的SELEX技术,又叫指数富集配体的系统进化技术(Systematic Evolution of Ligands by Exponential Enrichment,SELEX),是一种体外筛选技术,它具有筛选效率高、亲和特异性好,靶分子范围广等优点[7-9],在生物检测、药物开发和疾病诊断等领域都有广泛应用[10-13]。SELEX技术早期主要用于筛选对靶标有较高亲和特异性的寡核苷酸分子,即核酸适配体,最近发现SELEX技术在DNA核酶的筛选方面也具有较好的应用。目前采用该技术已经成功筛选出了上百种具有各种催化功能的DNA核酶,有些DNA核酶的催化能力甚至可以与蛋白质类酶相媲美,这大大丰富了核酶家族。为更好的了解、掌握和开发利用DNA核酶,本文将从DNA核酶的分类、筛选和应用等几方面对其最新进展进行介绍和分析。
1. DNA核酶的分类及其催化作用
按照催化类型可将DNA核酶分为切割类、连接类、磷酸化类和其他类,相应的底物、催化方式及代表性的DNA核酶如表1所示,其中切割类和连接类占的比例较大,也研究较多,下面对这些DNA核酶进行分类介绍。
表 1 DNA核酶的分类Table 1. Classification of deoxyribozyme类型 催化底物 催化方式 代表性的DNA核酶 参考文献 切割类 RNA 水解RNA磷酸二酯键 10-23、8-17 [14-15] DNA 氧化裂解DNA磷酸二酯键 Class I、Class II、RadDz3 [16-17] DNA 水解DNA磷酸二酯键 I-R1、I-R2、II-R1 [18] 胸腺嘧啶二聚体 光解胸腺嘧啶二聚体 UV1C [19] 酯类和芳香酰胺 水解碳氧双键 8zc9、8zc30 [20] 有酰胺键的人造DNA 水解酰胺键 AmideAm1 [21] 连接类 RNA 连接形成RNA磷酸二酯键 7DE5、9DB1 [14,22] DNA 连接形成DNA磷酸二酯键 E47 [23] DNA和马来酰亚胺乙烷 连接形成碳碳双键 DAB22 [24] RNA和氨基酸 连接形成核肽键 Tyr1 [25-26] 磷酸化类 DNA DNA的脱氧核糖5′位磷酸化 ATP-2.1、DK1 [27-28] RNA和酪氨酸 RNA的核糖5′位去磷酸化 7FN216 [29-30] 其他类 DNA DNA的脱氧核糖5′位腺苷酸化 I类加帽 [31] 卟啉 Zn2+或Cu2+螯合到卟啉环中 PS5.M [32] DNA和赖氨酸 DNA的脱氧核糖5′位去酰基化 7FN221 [33] 1.1 切割类
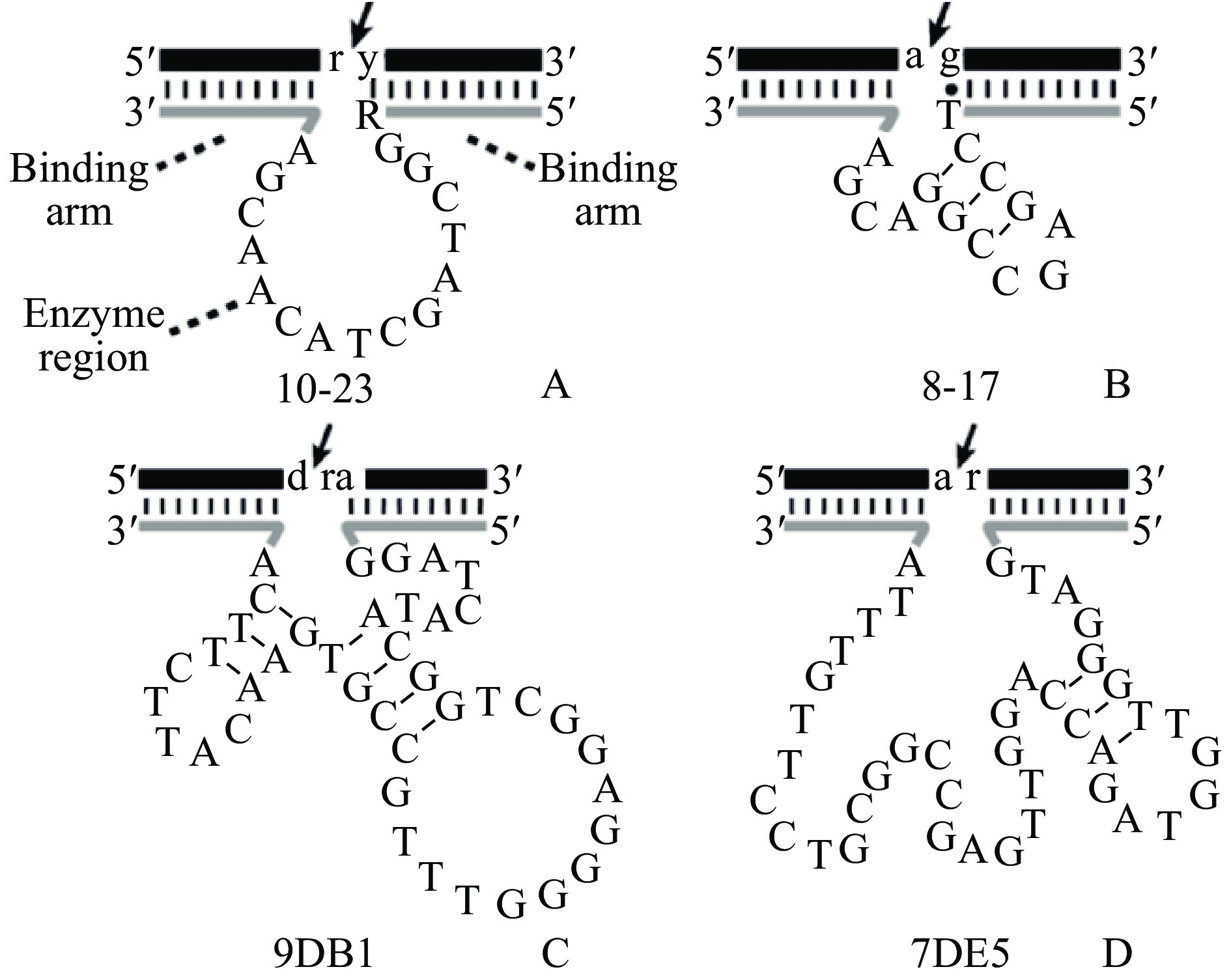
在切割RNA方面,比较经典的是10-23和8-17这两种DNA核酶,它们的催化机理目前已基本清楚(如图1A、B)[14]。它们能在Mg2+和Mn2+的辅助下使切割位点处的2′-羟基脱H+,形成的2′-氧阴离子,从而对其邻近的磷酸基发动亲核攻击,进而使其靶标RNA分子降解[14-15]。DNA核酶10-23理论上在人体生理条件下几乎可以切割所有的靶标RNA,具有极强的切割活性,其催化常数Kcat≈10 min−1,是目前已知最快的DNA核酶[15]。
在切割DNA方面,主要有Class I、Class II和RadDz3这三种代表性的DNA核酶,它们主要通过氧化裂解方式对底物DNA中的磷酸二酯键进行切割。Class I核酶是在Cu2+和抗坏血酸盐的辅助下进行催化,而Class II核酶则只需要Cu2+的辅助就可以进行催化[16],RadDz3核酶则不需要金属离子的辅助就能进行催化[17]。此外,Gu等[18]筛选出一系列能在Zn2+的辅助下快速水解DNA底物的DNA核酶I-R1、I-R2和II-R1,它们的作用位点也是底物DNA上的磷酸二酯键。自然条件下DNA要比RNA更加稳定,在生理条件下,DNA磷酸二酯键自然降解的半衰期为数百万年[18],而且DNA缺少2′-羟基,所以切割DNA要比切割RNA更加困难,相应核酶的催化机制也更为复杂。
在切割其他底物方面,有学者筛选出一种能光解胸腺嘧啶二聚体的DNA核酶UV1C,它可用较低能量的光激发发色基团,向胸腺嘧啶二聚体提供电子,使胸腺嘧啶二聚体不稳定,从而降解成胸腺嘧啶单聚体[19]。此外,Brandsen等[20]筛选出可催化水解酯类和芳香酰胺类化合物的DNA核酶,能够水解碳基类底物。Zhou等[21]则通过模拟蛋白质中的酰胺键,构建了一种含有酰胺键的DNA,进而筛选出可水解该人造DNA中酰胺键的DNA核酶,这些均表明DNA核酶在一定程度上具有替代蛋白质类酶的潜力。
总的看来,具有切割功能的DNA核酶,其切割底物主要有RNA、DNA、胸腺嘧啶二聚体、酯类、芳香酰胺、以及有酰胺键的人造DNA,一般都是在金属离子的辅助下,通过水解、氧化裂解、光解等方式,断裂底物中的磷酸二酯键、胸腺嘧啶二聚体、C=O双键、酰胺键,从而实现对底物的切割。
1.2 连接类
DNA核酶可以催化RNA底物的连接反应,目前研究较多的具有连接RNA活性的DNA核酶主要有9DB1、7DE5、7Q10、7S11和9F7。其中DNA核酶9DB1和7DE5,可在Mg2+和Zn2+的辅助下形成3′,5′-磷酸二酯键快速连接RNA,相应的催化机理如图1C、D[14];另外几个DNA核酶7Q10、7S11和9F7则通过2′,5′-磷酸二酯键连接RNA分子形成套索状或分支型的RNA分子[14,22]。
在连接DNA方面,Cuenoud等[23]筛选出可在Zn2+或Cu2+条件下连接DNA的DNA核酶E47,该核酶能使底物的5′-羟基进攻另一底物的3′-磷酸咪唑基,形成3′, 5′-磷酸二酯键,从而使两条DNA底物连接在一起。
在连接其他底物方面,Chandra等[24]筛选出了可连接5′-磷酸化的DNA和马来酰亚胺乙烷的DNA核酶DAB22,该核酶能催化上述底物完成双分子Diels-Alder反应(狄尔斯-阿尔德,一种环加成反应),进而在两个底物间形成C=C双键实现对两个底物的连接。还有些学者报道了一种DNA核酶Tyr1,是通过催化酪氨酸(Tyr)或丝氨酸(Ser)侧链上的羟基与5′-三磷酸化的RNA反应,从而连接形成核肽键[25-26]。
具有连接功能的DNA核酶,其连接底物中通常都有RNA、DNA,一般都需要在金属离子的辅助下,连接底物形成3′, 5′-磷酸二酯键、2′, 5′-磷酸二酯键、C=C双键、核肽键等化学键,从而实现对底物的连接。
1.3 磷酸化类
除了具有切割和连接作用的DNA核酶之外,一些具有磷酸化修饰作用的DNA核酶也被筛选出来。有学者报道多种可自我磷酸化的DNA核酶ATP-2.1、DK1和DK2,它们可将γ-磷酸基团转移到DNA的5′-羟基上,从而实现DNA自身的磷酸化[27-28]。
与自我磷酸化对应的是去磷酸化,有学者筛选出具有酪氨酸激酶活性的DNA核酶,该核酶能使5′-三磷酸化RNA上的γ-磷酸基团转移到多肽链中酪氨酸的羟基上,从而使RNA去磷酸化[29-30]。
1.4 其他类
这类核酶主要包括能催化DNA自我腺苷酸化、卟啉环金属化、赖氨酸酰基化等DNA核酶。DNA自我腺苷酸化也称自盖帽反应,是一种DNA的自我修饰方式。Li等[31]报道一种DNA核酶可催化AMP连到DNA分子的5′-磷酸末端,形成盖帽DNA。之后他还报道一种DNA核酶能将平面卟啉扭曲成过渡态,然后使Zn2+和Cu2+螯合到卟啉环中,从而催化卟啉环金属化[32]。Yao等[33]则筛选出一种能使赖氨酸酰基化的DNA核酶,该核酶能将5′-戊二酰基化DNA上的戊二酰基转移到多肽链中赖氨酸的氨基上,从而使赖氨酸酰基化,这些都进一步扩大了DNA核酶的催化范围。
2. DNA核酶的筛选
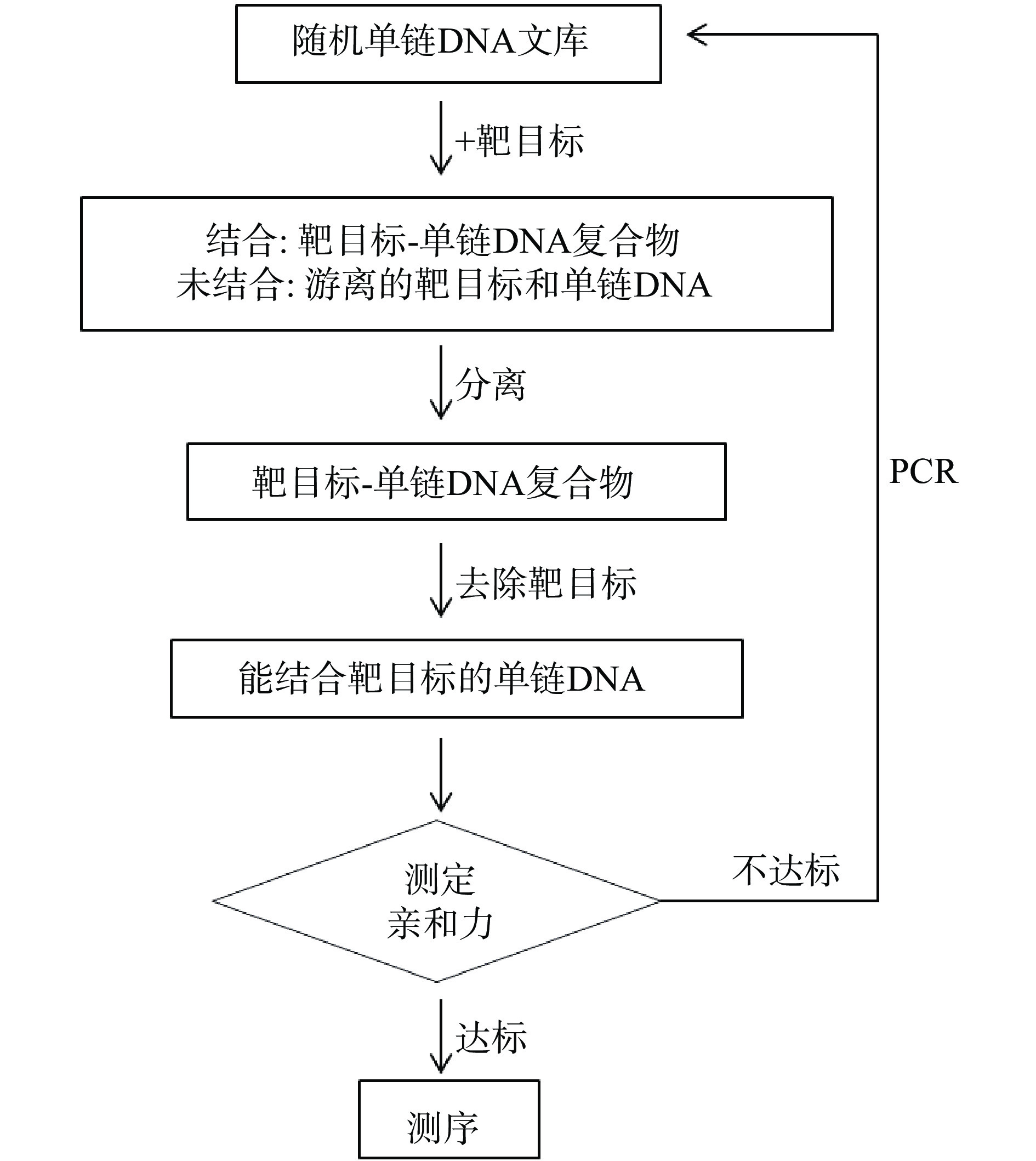
由于RNA和DNA都缺乏蛋白质中许多重要的蛋白官能团,而一些复杂、特殊的化学反应都需要这些官能团,因此DNA核酶展现的催化种类远少于蛋白质类酶[21,34-35]。目前,所有已经报道的DNA核酶都是利用SELEX技术筛选出来的,其基本筛选过程为建库、结合、分离、扩增和循环,相应的筛选流程如图2。传统SELEX筛选主要是为了获得对靶分子有较好亲和特异性的寡核苷酸分子,DNA核酶的SELEX筛选则是为了获得对靶分子有较好催化活性的寡核苷酸分子,二者的筛选目标和所要获得的活性分子是不同的,相应的二者的分离方法也有不少差别,传统的筛选通常采用加热变性的方法使具有活性的寡核苷酸分子空间结构变化从而与靶分子分离,对应的分离方法较多,而DNA核酶的SELEX筛选,有活性的寡核苷酸分子不仅要对靶分子有较好亲和特异性,还要具有催化靶分子的能力,因此核酶的筛选要求更高,相应活性分子的分离方式也较少,目前主要有两种分离方式,一种是利用生物素和链霉亲和素之间的偶联作用进行分离的,另一种则是采用聚丙烯酰胺凝胶电泳(PAGE电泳)分离的。下面分别以这两种分离方式为基础介绍DNA核酶的筛选。
2.1 生物素-链霉亲和素法分离筛选DNA核酶
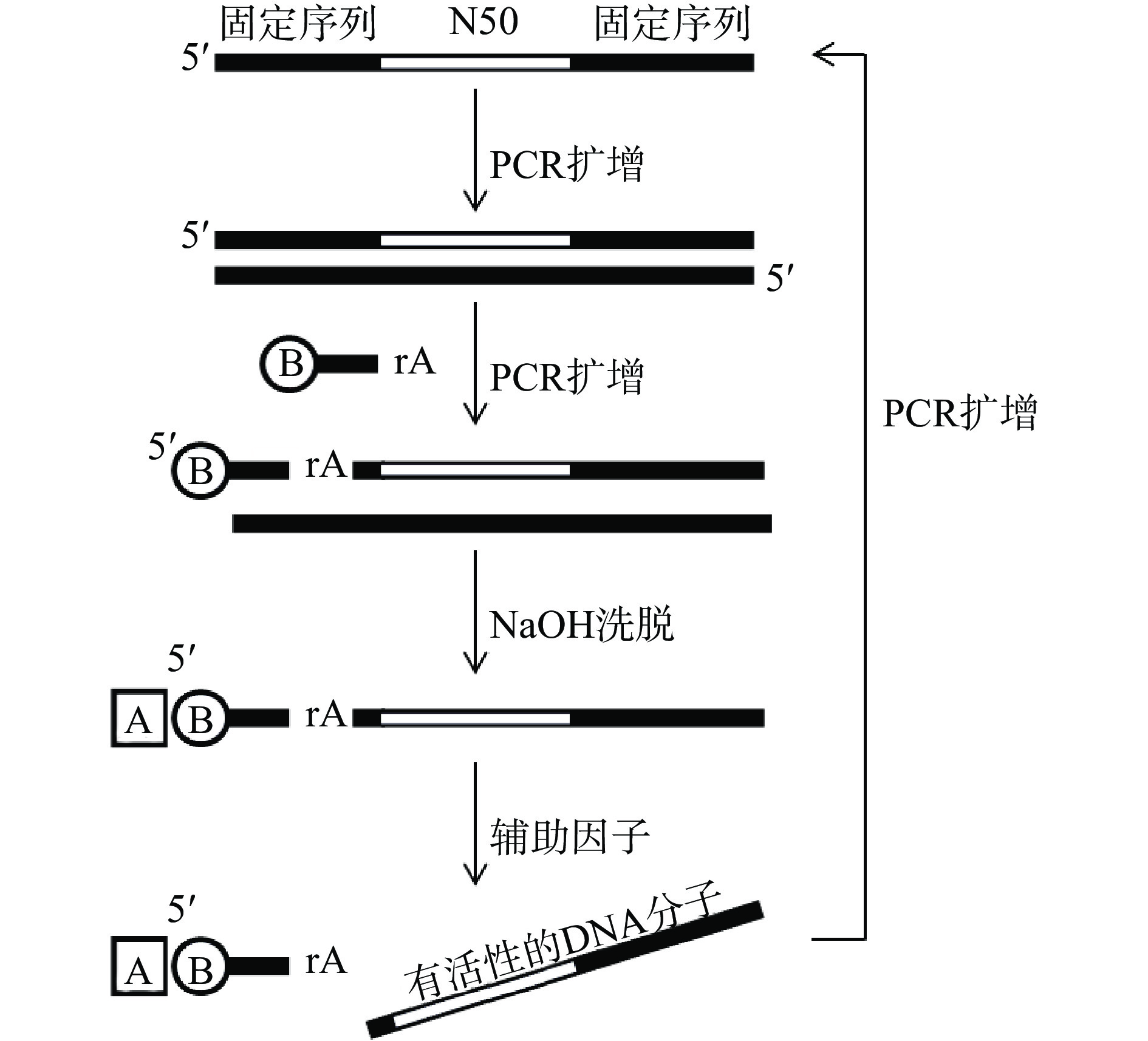
目前,大多数DNA核酶的筛选都是利用生物素和链霉亲和素之间的偶联作用来分离有催化活性的DNA核酶分子。许多学者利用此方法筛选出具有切割RNA活性的DNA核酶,具体筛选原理如图3[14,35-36]。首先合成一个两端为引物结合序列(固定序列)、中间为50个随机序列(N50)的单链DNA初始文库,以该DNA文库为模板进行第一次PCR扩增,形成的双链DNA则再作为第二次扩增模板,用含有5′端标记生物素基团和3′末端为核糖腺苷酸(rA)的DNA引物进行第二次PCR扩增,则生成含有rA的DNA产物,其中的rA就是核酶切割的靶点。之后利用生物素和链霉亲和素之间的偶联作用,将该DNA产物固定在有链霉亲和素的载体上,再加入NaOH溶液破坏该DNA产物,使其DNA双链解开,则未标记生物素的那条DNA链被洗去,然后用含有辅助因子(如Mg2+等金属离子)的筛选缓冲液与载体上的DNA产物共同孵育,Mg2+会使相应的DNA链折叠成活性结构,并在rA处进行切割,从而使有活性的DNA分子从载体上脱落下来,而没有活性的DNA分子则会继续保留在链霉亲和素的载体上。最后收集具有活性的DNA分子进行PCR,生成的PCR产物可作为次级文库进入下一轮的筛选。这样循环筛选之后,具有切割活性的DNA分子就会逐渐被富集,在DNA文库中的比例不断增加,一般筛选10~20轮即可获得具有切割活性的DNA核酶。目前利用这种分离方法已筛选到能催化RNA、DNA、胸腺嘧啶二聚体、卟啉等底物的DNA核酶,相关的核酶为10-23[14-15]、8-17[14-15]、Class I/II[16]、RadDz3[17]、I-R 1/2[18]、UV1C[19]、E47[23]、PS5.M[32](见表1)。
2.2 PAGE电泳法分离筛选DNA核酶
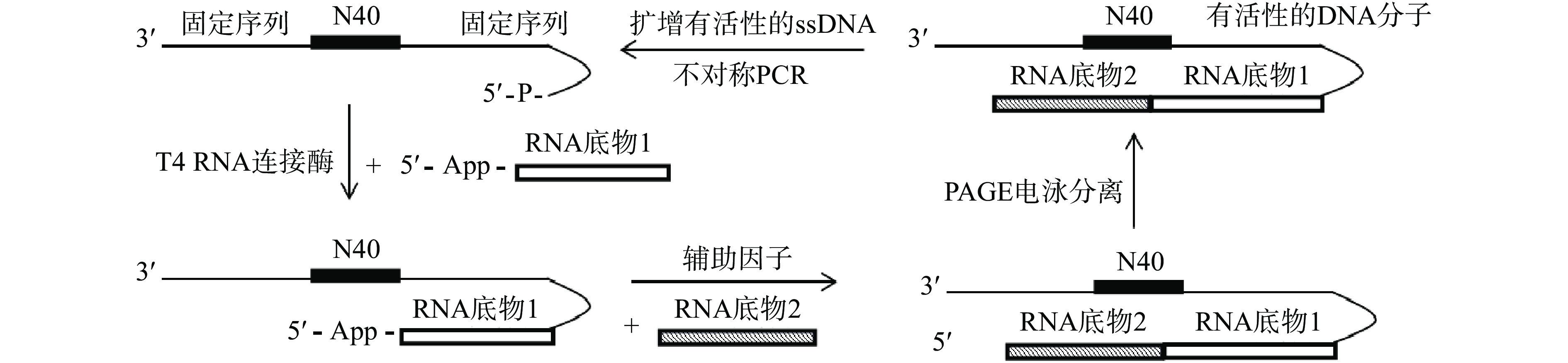
少数DNA核酶的筛选是利用聚丙烯酰胺凝胶电泳(Polyacrylamide Gel Electrophoresis,PAGE)来分离具有催化活性的DNA核酶分子。有学者利用此方法筛选出具有连接RNA活性的DNA核酶,具体筛选原理如图4[37]。首先利用T4 RNA连接酶将5′-腺苷酸化的RNA(App-RNA),即底物1连接到含有40个随机序列(N40)的单链DNA初始文库的5′端,然后在含有辅助因子(如Mn2+等金属离子)的筛选缓冲液中,将RNA底物2和上述底物1-DNA初始文库复合物共同孵育,Mn2+等辅助因子会使相应的DNA链折叠成具有核酶活性的结构,促使底物1和底物2的连接。然后PAGE电泳可根据分子量大小的不同将分子量较大的连接有两个RNA底物的、具有催化活性的DNA分子分离出来,再通过引物对其中有催化活性的DNA分子进行不对称PCR,从而获得大量的活性单链DNA,最后将这些活性单链DNA分子再次连接到底物1上,进入下一轮筛选。如此循环筛选可获得相应的有催化活性的DNA分子,即DNA核酶。目前利用这种分离方法已筛选到能催化RNA、DNA、酯类、芳香酰胺、氨基酸等底物的一系列DNA核酶(见表1)。
目前,DNA核酶的SELEX筛选基本上都是采用以上两种方式分离有核酶活性的DNA分子,其中生物素-链霉亲和素法属于DNA核酶筛选中的传统分离方式,常应用于核酸底物的核酶筛选;PAGE电泳分离法则是近年来新发展出的一种分离方式,较多应用于非核酸底物的核酶筛选,如蛋白质和多肽等底物,这也是学者们更加关注的方向。近年来,通过PAGE电泳的SELEX技术筛选出了许多非核酸类底物的DNA核酶,大大丰富了DNA核酶的催化种类。
3. DNA核酶的主要应用
3.1 在体内外金属离子检测中的应用
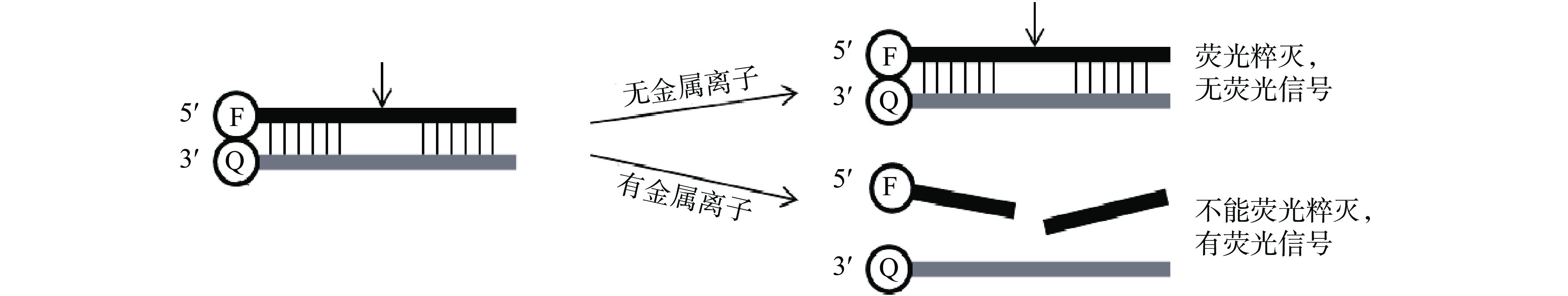
多数DNA核酶都需要依靠金属离子才能发挥其催化活性,这个特点使DNA核酶在体内外金属离子的检测中得到较好的应用。DNA核酶常与荧光粹灭基团联用检测体外金属离子,其检测原理如图5。在核酶的3′端标记有荧光淬灭基团Q,底物RNA的5′端则标记有荧光基团F,当检测体系中不存在要检测的金属离子时,DNA核酶与底物RNA成互补双链状态,此时荧光基团和荧光淬灭基团非常近,会导致最大化的荧光淬灭。而当检测体系中存在要检测的金属离子时,该DNA核酶会将底物切割成两个片段,导致荧光基团和荧光淬灭基团的分离,从而产生荧光信号[38-40]。目前利用该原理已经构建出多种荧光型传感器,实现对Na+[41]、Cu2+[42]和Pb2+[43]等多种金属离子的检测。随着纳米材料的开发,许多学者将其联用到DNA核酶上,如利用纳米金颗粒(Gold Nanoparticle,AuNPs)的显色变化与核酶联用对Pb2+进行检测[44];利用氧化石墨烯(Graphene Oxide,GO)作为荧光淬灭基团与核酶联用对Pb2+进行检测[45]。
对体内金属离子的检测,目前的报道还较少。而利用DNA核酶则可以检测斑马鱼的胚胎和幼体内的金属离子,该检测技术的原理与体外金属离子的检测类似,也是依据荧光淬灭原理进行设计的。利用近红外光对活体细胞损伤小和穿透能力强的特点,研究人员设计了一种底物-DNA核酶-纳米材料的复合物,DNA核酶与其底物成互补双链状态。当该复合物受到近红外光的照射时,纳米材料会受热分解,将核酶-底物复合物从纳米材料上释放到活体环境内,如果环境中有Zn2+,核酶则会在Zn2+的作用下切割底物,由于核酶与底物是根据上述荧光淬灭原理设计的,因此当底物被切割后,就会有荧光信号产生,从而实现对斑马鱼活体内Zn2+的检测[46]。
3.2 在药物治疗中的应用
最初应用于抗病毒和肿瘤的工具是RNA核酶,它们最大的功能就是剪切靶标RNA,利用这一特性,可以抑制mRNA的转录和翻译,使基因的表达受到抑制,从而达到药物治疗的目的。
DNA核酶10-23是目前最有潜力的可应用于药物治疗的工具酶。它具有极强的切割活性,而它的底物结合臂又具有很好的包容性,能与多种病毒的RNA结合,从而能较好地实现对病毒RNA的切割。大量文献都报道了它对各种靶病毒基因表达的抑制作用,尤其能抑制HIV病毒的基因表达,是一种较有潜力的治疗药物[47]。此外,Fan等[48]利用纳米材料构建了一种MnO2纳米给药体系,将DNA核酶放到这种MnO2纳米片上可用于药物治疗;Zhang等[49]利用纳米材料与核酶偶联构建了一种复合物(DzNPs),可敲除肿瘤坏死因子mRNA,从而可抑制动脉粥硬化的发展,这也进一步促进了DNA核酶在药物治疗中的应用。
3.3 在DNA分子加密系统中的应用
有学者设计了一种基于DNA核酶的分子加密系统,该系统由编码、加密和解密3部分构成。他先将要加密的文本内容按照ASCII编码转化为二进制数字,此过程为编码;再设计一个二进制数字与DNA碱基序列相互对应的规则或对应表,这样这些二进制数字就可转化为对应的DNA序列形成密文,此过程为加密;接收者收到了含有该DNA序列的DNA文库后,利用手中能特异性识别密文序列的DNA核酶,对文库中的DNA进行切割、连接等加工操作,从DNA文库中分离出目的片段,然后通过测序得到对应的DNA序列,从而得到原来的加密文本,此过程为解密[50]。由于DNA分子中包含4种脱氧核苷酸,是较好的信息存储的载体,DNA核酶更具有较高的特异性识别能力,是较好的解密钥匙,因此,与传统加密系统相比,DNA分子加密系统具有容量大和破译技术难等优势[51]。但目前仍然存在一些弊端,如解密过程中出现的非特异性伪降解等问题。但作为一个新的研究方向,该加密技术仍展现出了较大的应用前景。
4. 展望
DNA核酶的发展经历了一个从无到有,从简单到复杂,从催化单一核酸底物的水解反应到催化多种底物的多种反应,越来越多具有多种功能的DNA核酶被筛选出。但与蛋白质类酶相比,DNA核酶的种类还较少,大多数DNA核酶的底物都还是局限于核酸,因此,进一步筛选DNA核酶,尤其是筛选能催化更多类型底物的DNA核酶,是未来DNA核酶研究的一个重要任务;研究探索DNA核酶的催化机制,其催化活性与其空间折叠结构的关系,也是未来DNA核酶的一个研究方向;此外,随着纳米、稀土和石墨烯等新材料的兴起,未来很可能会将DNA核酶与这些新材料联系到一起应用于纳米机器人和生物传感等相关领域。相信未来人们对DNA核酶的研究定会迈入更高的层次。
-
表 1 DNA核酶的分类
Table 1 Classification of deoxyribozyme
类型 催化底物 催化方式 代表性的DNA核酶 参考文献 切割类 RNA 水解RNA磷酸二酯键 10-23、8-17 [14-15] DNA 氧化裂解DNA磷酸二酯键 Class I、Class II、RadDz3 [16-17] DNA 水解DNA磷酸二酯键 I-R1、I-R2、II-R1 [18] 胸腺嘧啶二聚体 光解胸腺嘧啶二聚体 UV1C [19] 酯类和芳香酰胺 水解碳氧双键 8zc9、8zc30 [20] 有酰胺键的人造DNA 水解酰胺键 AmideAm1 [21] 连接类 RNA 连接形成RNA磷酸二酯键 7DE5、9DB1 [14,22] DNA 连接形成DNA磷酸二酯键 E47 [23] DNA和马来酰亚胺乙烷 连接形成碳碳双键 DAB22 [24] RNA和氨基酸 连接形成核肽键 Tyr1 [25-26] 磷酸化类 DNA DNA的脱氧核糖5′位磷酸化 ATP-2.1、DK1 [27-28] RNA和酪氨酸 RNA的核糖5′位去磷酸化 7FN216 [29-30] 其他类 DNA DNA的脱氧核糖5′位腺苷酸化 I类加帽 [31] 卟啉 Zn2+或Cu2+螯合到卟啉环中 PS5.M [32] DNA和赖氨酸 DNA的脱氧核糖5′位去酰基化 7FN221 [33] -
[1] KRUGER K, GRABOWSKI P J, ZAUG A J, et al. Self-splicing RNA: Autoexcision and autocyclization of the ribosomal RNA intervening sequence of Tetrahymena[J]. Cell,1982,31(1):147−157. doi: 10.1016/0092-8674(82)90414-7
[2] GUERRIER-TAKADA C, GARDINER K, MARSH T, et al. The RNA moiety of ribonuclease P is the catalytic subunit of the enzyme[J]. Cell,1983,35(3):849−857. doi: 10.1016/0092-8674(83)90117-4
[3] ROBERTSOND L, JOYCE G F. Selection in vitro of an RNA enzyme that specifically cleaves single-stranded DNA[J]. Nature,1990,344(6265):467−468. doi: 10.1038/344467a0
[4] STRECKEROVA T, KURFURSTJ, CURTIS E A. Single-round deoxyribozyme discovery[J]. Nucleic Acids Research,2021,49(12):6971−6981. doi: 10.1093/nar/gkab504
[5] PONCE S A, BOCCALETTO P, BUJNICKI J M. DNAmoreDB, a database of DNAzymes[J]. Nucleic Acids Research,2021,49(D1):D76−D81. doi: 10.1093/nar/gkaa867
[6] BREAKER R R, JOYCE G F. A DNA enzyme that cleaves RNA[J]. Chemistry & Biology,1994,1(4):223−229.
[7] ZHANG D P, WANG H I. Fluorescence anisotropy reduction of an allosteric G-rich oligonucleotide for specific silver ion and cysteine detection based on the G-Ag+-G base pair[J]. Analytical Chemistry,2019,91(22):14538−14544. doi: 10.1021/acs.analchem.9b03556
[8] ZHU C, ZHAO X Y, YANG G, et al. Capillary electrophoresis involving in high efficiency screening for aptamers[J]. Chinese Journal of Analytical Chemistry,2020,48(5):583−589. doi: 10.1016/S1872-2040(20)60014-7
[9] WANG H Y, LI X, LAI L A, et al. X-aptamers targeting Thy-1 membrane glycoprotein in pancreatic ductal adenocarcinoma[J]. Biochimie,2021,181:25−33. doi: 10.1016/j.biochi.2020.11.018
[10] LIU H M, HAO J M, XU J, et al. Selection and identification of common aptamers against both Vibrio harveyi and Vibrio alginolyticus[J]. Chinese Journal of Analytical Chemistry,2020,48(5):623−631. doi: 10.1016/S1872-2040(20)60018-4
[11] ZHENG Y, ZHAO Y W, DI Y, et al. DNA aptamers from whole-serum SELEX as new diagnostic agents against gastric cancer[J]. RSC Advances,2019,9(2):950−957. doi: 10.1039/C8RA08642G
[12] SUN C Y, SU R F, BIE J X, et al. Label-free fluorescent sensor based on aptamer and thiazole orange for the detection of tetracycline[J]. Dyes and Pigments,2018,149:867−875. doi: 10.1016/j.dyepig.2017.11.031
[13] WANG T, CHEN C, LARCHER L M, et al. Three decades of nucleic acid aptamer technologies: Lessons learned, progress and opportunities on aptamer development[J]. Biotechnology Advances,2019,37(1):28−50. doi: 10.1016/j.biotechadv.2018.11.001
[14] BAUM D A, SILVERMAN S K. Deoxyribozymes: Useful DNA catalysts in vitro and in vivo[J]. Cellular & Molecular Life Sciences Cmls,2008,65(14):2156−2174.
[15] ROSENBACH H, BORGGRÄFE J, VICTOR J, et al. Influence of monovalent metal ions on metal binding and catalytic activity of the 10-23 DNAzyme[J]. Biological Chemistry,2021,402(1):99−111.
[16] WANG Y, YANG F, YANG X. Label-free colorimetric biosensing of copper (II) ions with unimolecular self-cleaving deoxyribozymes and unmodified gold nanoparticle probes[J]. Nanotechnology,2010,21(20):205502. doi: 10.1088/0957-4484/21/20/205502
[17] LEE Y, KLAUSER P C, BRANDSEN B M, et al. DNA-catalyzed DNA cleavage by a radical pathway with well-defined products[J]. Journal of the American Chemical Society,2017,139(1):255−261. doi: 10.1021/jacs.6b10274
[18] GU H, FURUKAWA K, WEINBERG Z, et al. Small, highly active DNAs that hydrolyze DNA[J]. Journal of the American Chemical Society,2013,135(24):9121−9129. doi: 10.1021/ja403585e
[19] BARLEV A, SEKHON G S, BENNET A J, et al. DNA repair by DNA: The UV1C DNA zyme catalyzes photoreactivation of cyclobutane thymine dimers in DNA more effectively than their de novo formation[J]. Biochemistry,2016,55(43):6010−6018. doi: 10.1021/acs.biochem.6b00951
[20] BRANDSEN B M, HESSER A R, CASTNER M A, et al. DNA-catalyzed hydrolysis of esters and aromatic amides[J]. Journal of the American Chemical Society,2013,135(43):16014−16017. doi: 10.1021/ja4077233
[21] ZHOU C, AVINS J L, KLAUSER P C, et al. DNA-catalyzed amide hydrolysis[J]. Journal of the American Chemical Society,2016,138(7):2106−2109. doi: 10.1021/jacs.5b12647
[22] WANG Y M, SILVERMAN S K. Directing the outcome of deoxyribozyme selections to favor native 3'-5' RNA ligation[J]. Biochemistry,2005,44(8):3017−3023. doi: 10.1021/bi0478291
[23] CUENOUD B, SZOSTAK J W. A DNA metalloenzyme with DNA ligase activity[J]. Nature,1995,375(6532):611−614. doi: 10.1038/375611a0
[24] CHANDRA M, SILVERMAN S K. DNA and RNA can be equally efficient catalysts for carbon-carbon bond formation[J]. Journal of the American Chemical Society,2008,130(10):2936−2937. doi: 10.1021/ja7111965
[25] WONG O Y, PRADEEPKUMAR P I, SILVERMAN S K. DNA-catalyzed covalent modification of amino acid side chains in tethered and free peptide substrates[J]. Biochemistry,2011,50(21):4741−4749. doi: 10.1021/bi200585n
[26] CHU C C, WONG O Y, SILVERMAN S K. A generalizable DNA-catalyzed approach to peptide-nucleic acid conjugation[J]. ChemBioChem,2014,15(13):1905−1910. doi: 10.1002/cbic.201402255
[27] LI Y F, BREAKER R R. Phosphorylating DNA with DNA[J]. Proceedings of the National Academy of Sciences,1999,96(6):2746−2751. doi: 10.1073/pnas.96.6.2746
[28] MCMANUS S A, LI Y F. Multiple occurrences of an efficient self-phosphorylating deoxyribozyme motif[J]. Biochemistry,2007,46(8):2198−2204. doi: 10.1021/bi061613c
[29] WALSH S M, SACHDEVA A, SILVERMAN S K. DNA catalysts with tyrosine kinase activity[J]. Journal of the American Chemical Society,2013,135(40):14928−14931. doi: 10.1021/ja407586u
[30] CHANDRASEKAR J, WYLDER A C, SILVERMAN S K. Phosphoserine lyase deoxyribozymes: DNA-catalyzed formation of dehydroalanine residues in peptides[J]. Journal of the American Chemical Society,2015,137(30):9575−9578. doi: 10.1021/jacs.5b06308
[31] LI Y F, LIU Y, BREAKER R R. Capping DNA with DNA[J]. Biochemistry,2000,39(11):3106−3114. doi: 10.1021/bi992710r
[32] LI Y F, SEN D. Toward an efficient DNAzyme[J]. Biochemistry,1997,36(18):5589−5599. doi: 10.1021/bi962694n
[33] YAO T J, PRZYBYLA J J, YEH P, et al. DNAzymes for amine and peptide lysine acylation[J]. Organic & Biomolecular Chemistry,2020,19(1):171−181.
[34] HUANG P J J, LIU J. In vitro selection of chemically modified DNAzymes[J]. Chemistryopen,2020,9(10):1046−1059. doi: 10.1002/open.202000134
[35] 佟宗轩, 胡沁沁, 顾宏周. DNA酶: 筛选, 生物传感及展望[J]. 高等学校化学学报,2020,41(11):2345−2355. [TONG Z X, HU Q Q, GU H Z. Deoxyribozymes: Selection, biosensing and outlook[J]. Chemical Journal of Chinese Universities-Chinese,2020,41(11):2345−2355. [36] 王月瑶. 催化RNA切割反应的新型短结合臂脱氧核酶[D]. 南京: 南京大学, 2019. WANG Y Y. A novel small RNA-cleaving deoxyribozyme with a short binding arm[D]. Nanjing: Nanjing University, 2019.
[37] SCHEITL C P M, LANGE S, HOBARTNER C. New deoxyribozymes for the native ligation of RNA[J]. Molecules,2020,25(16):3650. doi: 10.3390/molecules25163650
[38] MORRISON D, ROTHENBROKER M, LI Y F. DNAzymes: Selected for applications[J]. Small Methods,2018,2(3):1700319. doi: 10.1002/smtd.201700319
[39] SILVERMAN S K. Catalytic DNA: Scope, applications, and biochemistry of deoxyribozymes[J]. Trends in Biochemical Sciences,2016,41(7):595−609. doi: 10.1016/j.tibs.2016.04.010
[40] ZHANG X B, KONG R M, LU Y. Metal ion sensors based on DNAzymes and related DNA molecules[J]. Annual Review of Analytical Chemistry,2011,4:105−128. doi: 10.1146/annurev.anchem.111808.073617
[41] TORABI S F, WU P, MCGHEE C E, et al. In vitro selection of a sodium-specific DNAzyme and its application in intracellular sensing[J]. Proceedings of the National Academy of Sciences,2015,112(19):5903−5908. doi: 10.1073/pnas.1420361112
[42] LI H, HUANG X X, KONG D M, et al. Ultrasensitive, high temperature and ionic strength variation-tolerant Cu2+ fluorescent sensor based on reconstructed Cu2+-dependent DNAzyme/substratecomplex[J]. Biosensors and Bioelectronics,2013,42:225−228. doi: 10.1016/j.bios.2012.10.070
[43] LI H, ZHANG Q, CAI Y, et al. Single-stranded DNAzyme-based Pb2+ fluorescent sensor that can work well over a wide temperature range[J]. Biosensors and Bioelectronics,2012,34(1):159−164. doi: 10.1016/j.bios.2012.01.037
[44] MOON W J, LIU J. Interfacing catalytic DNA with nanomaterials[J]. Advanced Materials Interfaces,2020,7(21):2001017. doi: 10.1002/admi.202001017
[45] ZHAO X H, KONG R M, ZHANG X B, et al. Graphene-DNAzyme based biosensor for amplified fluorescence “turn-on” detection of Pb2+ with a high selectivity[J]. Analytical Chemistry,2011,83(13):5062−5066. doi: 10.1021/ac200843x
[46] YANG Z L, LOH K Y, CHU Y T, et al. Optical control of metal ion probes in cells and zebrafish using highly selective DNAzymes conjugated to upconversion nanoparticles[J]. Journal of the American Chemical Society,2018,140(50):17656−17665. doi: 10.1021/jacs.8b09867
[47] 范思思, 程进, 冀斌, 等. 脱氧核酶在生物检测及基因治疗中的研究进展[J]. 科学通报,2019,64:1027−1036. [FAN S S, CHEN J, JI B, et al. DNAzymes in biological detection and gene therapy[J]. Chin Sci Bull,2019,64:1027−1036. doi: 10.1360/N972018-00874 [48] FAN H, ZHAO Z, YAN G, et al. A smart DNAzyme-MnO2 nanosystem for efficient gene silencing[J]. Angewandte Chemie,2015,127(16):4883−4887. doi: 10.1002/ange.201411417
[49] ZHANG J H, MA R, BLANCHARD A, et al. Conditional deoxyribozyme-nanoparticle conjugates for miRNA-triggered gene regulation[J]. ACS Applied Materials & Interfaces,2020,12(34):37851−37861.
[50] 李一凡, 吴燃峰, 杨静, 等. 基于DNA核酶的分子加密系统[J]. 信息网络安全,2017(6):43−48. [LI YF, WU R F, YANG J, et al. A molecule encryption system based on DNAzyme[J]. Netinfo Security,2017(6):43−48. doi: 10.3969/j.issn.1671-1122.2017.06.007 [51] 彭维平, 程丹华, 宋成. 基于多碱基组合映射编码和DNA计算的一次一密算法[J]. 计算机应用研究,2019,36(7):2190−2194. [PENG W P, CHENG D, SONG C. A one-cipher algorithm based on multi-base combination mapping coding and DNA calculation[J]. Application Research of Computers,2019,36(7):2190−2194. doi: 10.19734/j.issn.1001-3695.2018.01.0100





 下载:
下载:
 下载:
下载:



