Protective Effects of Enzymatic Products from Sturgeon Roe on Alcohol-induced Hepatic Cell Damage and Virtual Screening of Active Peptides
-
摘要: 本研究旨在探究鲟鱼子酶解产物对酒精损伤肝细胞的保护作用,并深入阐明其作用机理。以鲟鱼子为研究对象,结合酶解效率和体外活性等关键指标,对其酶解工艺进行优化。借助酒精损伤HepG2细胞模型,系统研究鲟鱼子酶解产物对肝细胞的保护作用。运用计算机虚拟筛选技术,探索潜在的生物活性多肽序列。研究结果表明,在碱性蛋白酶(1343 U/g)及胰酶(27 U/g)1:1复配酶解8 h的条件下获得的鲟鱼子酶解产物最优,蛋白回收率为49.30%±0.57%,水解度为46.05%±0.92%,ABTS+自由基清除率为51.45%±0.66%。不同浓度下均表现出显著的乙醇脱氢酶(Alcohol Dehydrogenase,ADH)激活率(P<0.05),在5 mg/mL时为168.64%±1.42%。在此酶解条件下制备的产物,0.3~2 mg/mL时与模型组相比能显著提升酒精损伤HepG2细胞内超氧化物歧化酶(Superoxide Dismutase,SOD)活性、谷胱甘肽(Glutathione,GSH)含量(P<0.05),显著降低丙二醛(Malondialdehyde,MDA)含量(P<0.05)。此外,酶解产物在0.3~2 mg/mL时显著降低丙氨酸氨基转移酶(Alanine Aminotransaminase,ALT)和天门冬氨酸氨基转移酶(Aspartate Aminotransferase,AST)的活性(P<0.05)。虚拟筛选结果显示,鲟鱼子酶解产物中的LPG和FLPR等5条多肽显示潜在的酒精损伤肝细胞保护作用。因此,本研究为进一步发展鲟鱼子等水产原料的精深加工利用提供了基础支持。Abstract: This study was designed to explore the hepatoprotective effects of enzymatic degradation products derived from sturgeon roe on alcohol-damaged hepatocytes and to elucidate the underlying mechanisms. Utilizing sturgeon roe as the research material, the enzymatic process was optimized by focusing on key parameters such as enzymatic efficiency and in vitro activity. The protective effects on hepatocytes were systematically investigated by using the HepG2 cell model. Advanced computerized virtual screening technology was employed to identify potential bioactive peptides within the sturgeon roe. The findings indicated that the optimum enzymatic product of sturgeon roe was obtained under the conditions of 1:1 compounding of alkaline protease (1343 U/g) and trypsin (27 U/g) for 8 h, yielded a protein recovery of 49.30%±0.57%, a hydrolysis degree of 46.05%±0.92%, and ABTS+ free radical scavenging rate of 51.45%±0.66%. Notably, at a concentration of 5 mg/mL, this product significantly enhanced the activity of alcohol dehydrogenase (ADH) by 168.64%±1.42% (P<0.05). The product prepared under this enzymatic condition at 0.3~2 mg/mL significantly elevated superoxide dismutase (SOD) activity, glutathione (GSH) contents, and reduced malondialdehyde (MDA) contents in alcohol-injured HepG2 cells compared to the model group (P<0.05). In addition, the product at 0.3~2 mg/mL also significantly reduced alanine aminotransferase (ALT) and aspartate aminotransferase (AST) activities (P<0.05). Virtual screening identified 5 peptides, including LPG and FLPR, in the sturgeon roe enzymatic degradation product, showed promising hepatoprotective properties against alcohol-induced hepatocyte injury. Consequently, this study lays a solid foundation for the further development and utilization of aquatic resources, such as sturgeon roe, in hepatoprotective applications.
-
Keywords:
- sturgeon /
- sturgeon roe /
- alcohol dehydrogenase /
- antioxidation /
- bioactive peptides /
- alcohol metabolism
-
鲟鱼是一种拥有超过2亿年历史的硬骨鱼类,被誉为鱼类中的“活化石”。这种古老的鱼品种的每一部分都有其价值,尤其是鲟鱼子等副产物,富含蛋白质、人体必需的氨基酸、不饱和脂肪酸、无机盐,以及如铜、镁、钙和硒等的微量元素[1],因此被誉为“黑色黄金”[2]。有研究表明,鲟鱼子对于人体的心脑血管相关疾病和矿物质调节等具有很好的健康效应[3]。目前对于鲟鲟鱼子的加工,多集中于鲟鱼子酱等高价值产品,催生了鲟鱼子从野生鱼种到养殖鱼种的转变。然而,由于鲟鱼子原料的含水量和营养成分高等特点,鲟鱼子酱产品对鲟鱼子颗粒大小及储运等均具有极高的要求[4]。随着产量的增大,造成了部分鲟鱼子原料的浪费。因此,深度加工鲟鲟鱼子不仅能最大化地利用这一资源、实现高效利用,还能提高产业的附加值,从而推动鲟鱼养殖业的持续和健康发展。
酒精相关肝损伤(Alcohol-associated Liver Damage,ALD)是全球最常见且可预防的慢性疾病之一,与全球的高发病率和死亡率有关。其病理特征范围包括肝脏脂肪堆积,这进一步导致酒精相关的脂肪性肝炎、纤维化和肝硬化[5]。很多研究表明,长期和大量饮酒会导致肝毒性,从而增加慢性肝损伤的风险。近年来的研究表明ALD发病机制可能与多种因素有关,包括脂质代谢、氧化应激、炎症、细胞凋亡等[6−7]。由于缺乏药物治疗ALD的选择,ALD的治疗和预防仍然是全球主要的健康问题。
食源性蛋白质酶解产物由于其广泛的来源、简洁且环保的制备工艺以及多种生物活性,已成为科研领域的热点研究对象[8]。至今,多种蛋白酶解产物已被用于酒精性肝损伤的治疗和预防研究中[9−10]。研究表明,肝脏是主要的新陈代谢器官,它可以通过若干的酶促和非酶促途径将摄取的酒精90%以上转化为乙醛[11],有研究发现摄入乙醇后产生的诸多影响主要是通过乙醇的次级生成物乙醛来实现的,而这种乙醛主要由乙醇脱氢酶(ADH)、细胞色素P450 2E1(CYP2E1)和过氧化氢酶转化而来[12]。Xiao等[13]、Chen等[14]通过对酶解产物的抗炎抗氧化、ADH激活率等指标筛选出改善ALD症状的酶解产物。综上所述,通过酶解食源性蛋白质以获得具有解酒及保护肝脏功能的生物活性多肽是一种有效的策略[15]。
因此,本研究以具有较高蛋白质含量的鲟鱼鱼子为研究对象,通过限制性酶解技术,借助体外抗氧化和ADH激活能力等评价指标,得到具有潜在护肝功效的鱼子酶解产物,进而利用酒精损伤肝细胞(HepG2)模型,研究其改善细胞损伤的作用。并进一步利用质谱分析联合计算机虚拟筛选,得到鲟鱼子酶解产物中的潜在生物活性多肽序列信息。本研究将为鱼子酶解产物在解酒护肝产品中的应用奠定理论和技术基础。
1. 材料与方法
1.1 材料与仪器
新鲜鲟鱼鱼子 贵州省千鲟生物科技有限公司;胰酶(4000 U/g)、碱性蛋白酶(200 U/mg) 上海源叶生物科技有限公司;ADH、尼克酰胺腺嘌呤二核苷酸(NAD+)、甲酸(FA)、碳酸氢铵、二硫苏糖醇(DTT)、十二烷基硫酸钠(SDS)、邻苯二甲醛(OPA)、碘乙酰胺(IAA)及尿素等 美国Sigma-Aldrich公司;细胞存活率测定(CCK-8)、超氧化物歧化酶(SOD)、丙二醛(MDA)、谷胱甘肽(GSH)、丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)检测试剂盒 南京建成生物工程研究所;HepG2细胞 上海安为生物科技有限公司。
T25均质机 德国IKA公司;SHA-B恒温振荡器 上海力辰仪器科技有限公司;InfiniteM 200 Pro酶标仪 奥地利TECAN公司;高效液相色谱仪EASY-nanoLC 1200串联Q-Exactive Plus质谱仪、3110 Series二氧化碳培养箱 美国Thermo Fisher Scientific公司;Milli-Q 超纯水制备系统 美国 Millipore 公司。
1.2 实验方法
1.2.1 酶解流程及条件优化
10 g鲟鱼子样品以1:6的比例与去离子水混合,并在8000 r/min条件下进行1 min均质处理,实验条件由预实验结果确定。随后,样品的pH被调整至酶最适pH,并加入酶在55 ℃下进行酶解。为了终止酶解反应,样品在沸水浴中处理15 min。处理完毕后,样品冷却至室温后在4 ℃,8000 r/min的条件下离心取上清液用于水解度、蛋白回收率、ADH激活率、ABTS抗氧化指标的测定。−80 ℃条件下储存备用。
对于酶种类的单因素实验,胰酶(108 U)、碱性蛋白酶(5372 U)、以及胰酶(54 U)与碱性蛋白酶(2686 U)的1:1复配酶酶解4 h。在酶解时间的单因素实验中,采用胰酶(54 U)与碱性蛋白酶(2686 U)的1:1复配酶,考察酶解时间分别为2、4、8、12、16 h。对于加酶量的单因素实验,使用复配酶进行8 h酶解,考察复配酶分别添加0.2%(胰酶11 U+碱性蛋白酶537 U)、0.5%(胰酶27 U+碱性蛋白酶1343 U)、0.8%(胰酶43 U+碱性蛋白酶 2149 U)、1%(胰酶54 U+碱性蛋白酶2686 U)、2%(胰酶108 U+碱性蛋白酶5372 U)。
1.2.2 水解度及蛋白回收率测定
采用OPA法测定水解度,配制OPA工作液(50 mL工作液中含有1.905 g四硼酸钠、50 mg SDS、40 mg OPA及44 mg DTT)及1 mg/mL样品溶液。随后,向紫外96孔板中分别加入40 μL去离子水(空白组)、丝氨酸溶液(标品组)和样品溶液,并用排枪向其中加入300 μL OPA溶液。振荡混匀,精确反应2 min后在340 nm下测定其吸光度。水解度(DH)由公式(1)计算。鲟鱼子、酶解上清液蛋白含量采用GB 5009.5-2016《食品安全国家标准 食品中蛋白质的测定》中的凯氏定氮法测定。蛋白质回收率由公式(2)计算。
DH(%)=水解的肽键数总肽键数×100 (1) 蛋白回收率(%)=酶解上清液蛋白含量鲟鱼子蛋白含量×100 (2) 1.2.3 ADH激活率测定
根据Xiao等[16]的方法,并进行一定的修改。分别将样品浓度稀释至5 mg/mL后再梯度稀释至2.5、1 mg/mL,取稀释后样品50 μL与50 μL ADH(1 U/mL)混合溶液添加至石英96孔板中,双蒸水作为对照,在37 ℃恒温孵育箱中孵育20 min。将22.4 mmol/L焦磷酸钠、27 mmol/L NAD+、5%乙醇以3:2:1的比例混合,在37 ℃孵育5 min后向石英板孔中加入150 μL。用酶标仪每隔40 s检测340 nm吸光度值,检测20 min。拟合反应动力学曲线,计算斜率(K),根据式(3)得到ADH激活率。
ADH激活率(%)=K样品−K对照K对照×100 (3) 1.2.4 鲟鱼子酶解上清液抗氧化能力测定
参考Zhao等[17]的方法测定相同蛋白浓度酶解产物的ABTS+自由基清除能力。向50 μL蛋白浓度为0.15 mg/mL的样品溶液中加入150 μL ABTS溶液,反应混合液在30 ℃下保温30 min,测定其734 nm处的吸光度值,记为A样本。用50 μL PBS溶液代替样品溶液,作为对照组,吸光度值记为A对照。根据式(4)计算ABTS+自由基清除率。
ABTS+自由基清除率(%)=(1−A样本A对照)×100 (4) 1.2.5 HepG2细胞培养
HepG2细胞在DMEM培养基中,补充10%(v/v)胎牛血清下培养,并维持在37 ℃,5% CO2的条件下。当细胞覆盖率达到约80%时,进行细胞传代。
1.2.6 酒精诱导HepG2细胞损伤模型的建立
将对数生长期的HepG2细胞以2×104的密度接种于96孔培养板培养24 h。更换含有不同浓度(3%~8%)酒精的培养液继续培养24 h,每个浓度设6个复孔。弃上清液,分别加入100 μL含CCK-8的培养液,继续培养30 min后,使用酶标仪在450 nm处检测吸光度(A),利用公式(5)计算细胞相对活力。选择蛋白浓度为0.3、0.8、1、2 mg/mL的鲟鱼子酶解液检测细胞毒性范围,检测方法同酒精模型组。
细胞相对活力(%)=A酒精组A正常组×100 (5) 1.2.7 鲟鱼子酶解液保护酒精损伤肝细胞的细胞相对活力检测
细胞接种于96孔板培养24 h后,分别加入不同浓度鲟鱼子酶解上清液预处理24 h,各组加入终浓度6%乙醇诱导损伤,对照组加入等量培养基,37 ℃孵育24 h,弃上清液,分别加入100 μL含CCK-8的培养液,继续培养30 min后,使用酶标仪在450 nm处检测吸光度(A),并根据CCK-8试剂盒说明书测定细胞相对活力。
1.2.8 鲟鱼子酶解液对酒精诱导的HepG2细胞氧化应激及乙醇代谢相关酶活的影响
将HepG2细胞以每孔2×105/mL接种于6孔板中贴壁24 h后,弃上清,对照组、模型组加培养基,样品组用含有不同浓度样品(0.3、0.8、1.0和2.0 mg/mL)预处理24 h,再加入6%乙醇的培养基培养24 h后,收集细胞按照相关试剂盒说明书测定SOD、MDA、GSH水平。参照ALT、AST试剂盒方法测定细胞培养基中ALT、AST水平。细胞蛋白含量均采用BCA试剂盒测定。
1.2.9 nano-HPLC-MS/MS分析多肽序列
取适量酶解上清液冻干样本经C18除盐柱进行除盐。将样品经由配备在线纳喷离子源的HPLC-MS/MS分析。整套系统为串联EASY-nanoLC 1200的Q-Exactive Plus质谱仪。上样量为3 μL(分析柱:Acclaim PepMap C18,75 μm×25 cm),以60 min的梯度分离样品,柱流量控制在300 nL/min,柱温为40 ℃,电喷雾电压2 kV,梯度洗脱程序:0~46 min,2% B;47 min,35% B;47~48 min,100% B;48~60 min,100% B。
质谱仪在数据依赖采集模式下运行,自动在MS和MS/MS采集间切换。质谱参数设置:MS:扫描范围200~2000 m/z;分辨率为70000;AGC target为3e6;最大注入时间为50 ms。HCD-MS/MS:分辨率为17500;AGC target为1e5;最大注入时间45 ms;碰撞能量:28%;动态排除时间30 s。采用PEAKS Studio软件(加拿大BSI公司)处理得到多肽序列信息。
1.2.10 生物活性多肽虚拟筛选
在本研究中,使用Peptide Ranker(http://distilldeep.ucd.ie/PeptideRanker/)进行肽段的生物活性预测并根据其潜在生物活性进行评分排序,同时利用CPPpred(http://distilldeep.ucd.ie/CPPpred/)对肽段的细胞渗透性进行预测和排名。
以Peptide Ranker评分>0.5,CPPpred评分>0.2,以及相对峰面积>0.2%为筛选标准,从中挑选出具有潜在生物活性的肽段。进一步构建一个气泡图,其中Peptide Ranker评分为x轴、CPPpred评分为y轴,而肽的峰面积则决定气泡的大小,以此直观展示三者之间的关系。
使用PepDraw工具(http://www.tulane.edu/~biochem/WW/PepDraw/index.html)预测多肽的关键化学性质,包括等电点、净电荷以及疏水性。
1.3 数据处理
统计性分析采用SPSS 20.0软件完成。细胞实验数据通过GraphPad Prism 7.0软件进行处理与分析,所有数据结果均以均值±标准偏差形式表达。为识别不同组均值间的显著性差异,采用单因素方差分析(ANOVA)并结合Duncan的多重比较法,设定显著性水平为P<0.05和P<0.01。
2. 结果与分析
2.1 不同酶种类对鲟鱼子酶解效率及酶解液活性的影响
由于特异性原因,不同酶种类对鲟鱼子原料中蛋白质的酶切位点不同,会产生出不同的多肽序列,导致其水解度和蛋白质回收率的差异[18]。本研究采用胰酶、碱性蛋白酶及胰酶和碱性蛋白酶复配酶作为酶切制剂制备鲟鱼子酶解产物。其中,胰酶是常见消化用酶,它是胰腺释放的酶的混合物,优先切割与Arg、Lys、Tyr和Leu相关的肽键[19]。而碱性蛋白酶是源自林草芽孢杆菌(Bacillus licheniformis)的一种丝氨酸内肽酶[20]。
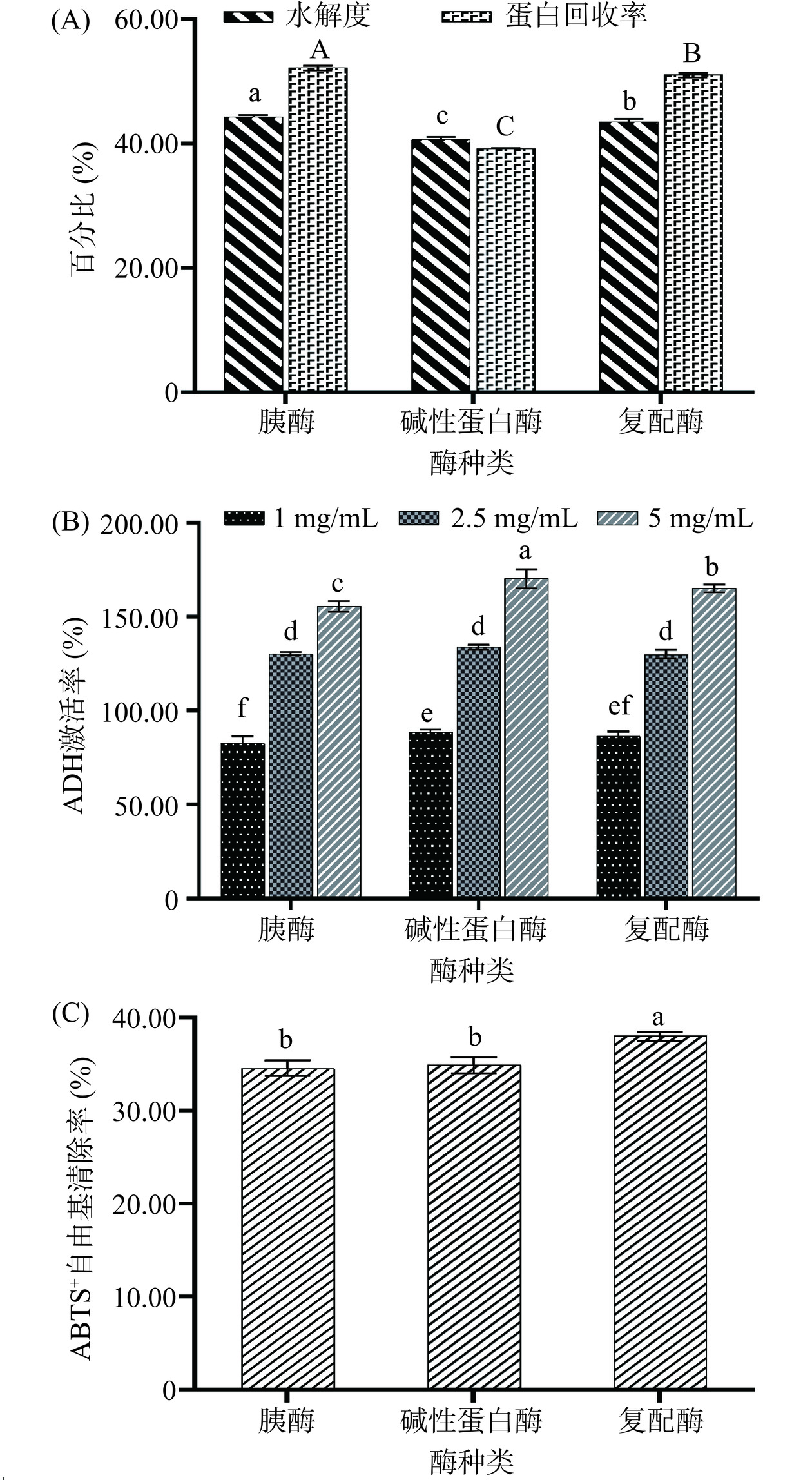
由图1(A)可知,不同酶种类得到的鲟鱼子酶解产物水解度从高到低依次是胰酶(44.27%±0.27%)、复配酶及碱性蛋白酶。蛋白回收率从高到低依次是胰酶(52.18%±0.29%)、复配酶及碱性蛋白酶。由此说明,胰酶作为多种酶混合物具有较高的酶解效率,复配酶及碱性蛋白酶次之。
由图1(B)可知,酶解产物蛋白含量在5 mg/mL时,碱性蛋白酶的ADH激活率为170.52%±4.79%,显著高于复配酶与胰酶(P<0.05);在1~2.5 mg/mL浓度下,碱性蛋白酶处理的酶解液ADH激活能力高于其他酶解液产物,但无显著性差异(P>0.05)。这是由于多肽的释放程度和序列差异,碱性蛋白酶和胰酶剪切位点的不同导致酶解产物表现出各自独特的生物活性[21]。Zan等[22]、Xiao等[13]分别采用碱性蛋白酶、中性蛋白酶、菠萝蛋白酶、风味蛋白酶、木瓜蛋白酶制备食源性ADH激活肽,发现碱性蛋白酶最适合用于制备ADH激活肽,这与本实验的研究结果一致。
由图1(C)可知,复配酶处理的酶解产物抗氧化能力(38.05%±0.42%)显著高于两种酶单独处理的酶解液(P<0.05),胰酶与碱性蛋白酶抗氧化能力无显著性差异(P>0.05)。因此,结合酶解产物的水解度、蛋白回收率、ADH激活率、ABTS+自由基清除率的实验结果选择综合效果都相对较好的复配酶(碱性蛋白酶:胰酶=1:1)为水解最佳用酶,对其酶解工艺条件继续进行优化。
2.2 不同酶解时间对鲟鱼子酶解效率及酶解液活性的影响
随着酶解时间的延长,酶解液中多肽的释放和交联呈现动态过程,进一步影响酶解效率及酶解液活性[23]。本研究考察复配酶处理下,不同酶解时间对鲟鱼子酶解效率及酶解液活性的影响。
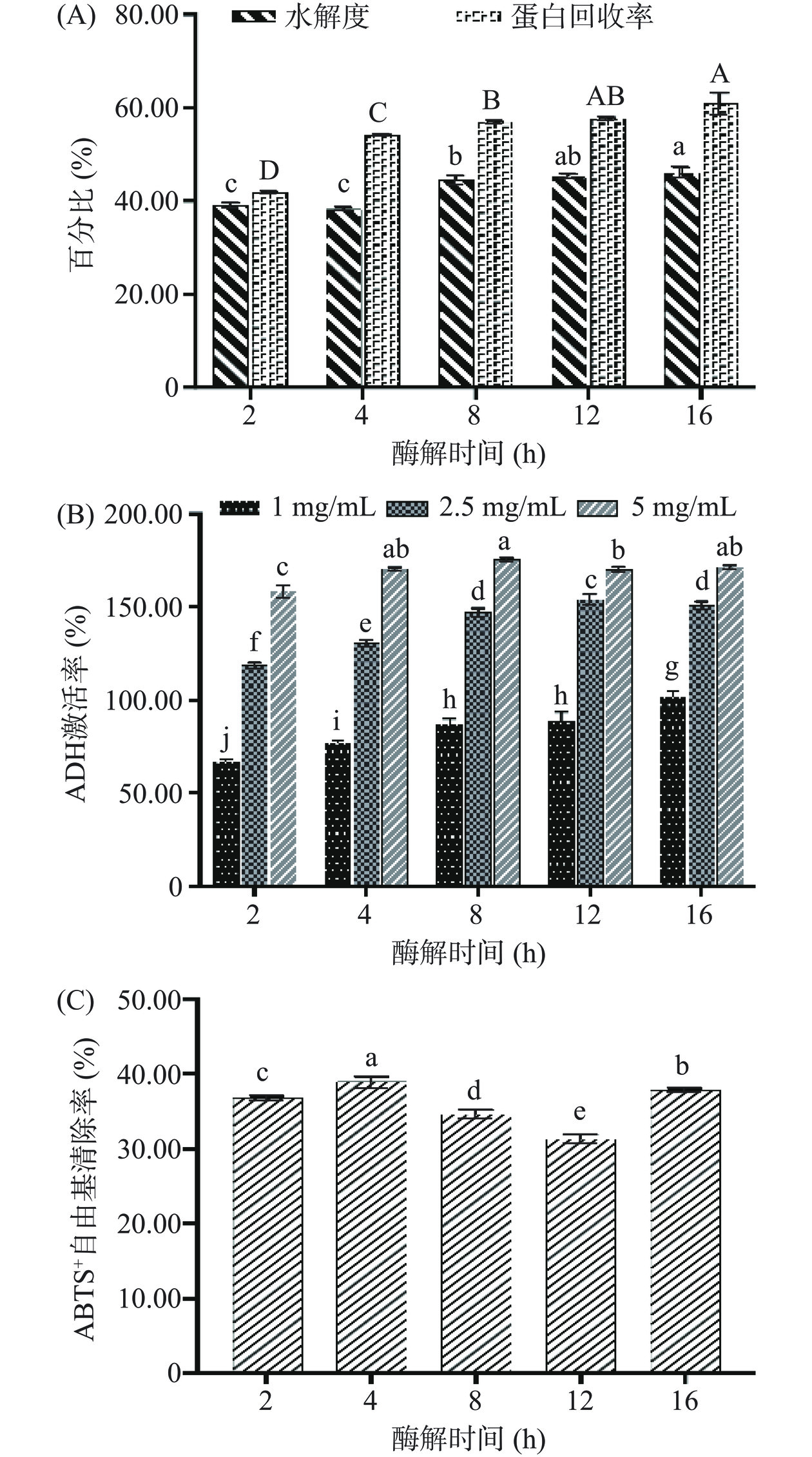
由图2(A)可知,随着酶解时间的延长,水解度呈现先增高后平缓的趋势,在酶解时间为8 h时达到较高水解度(44.43%±0.97%)。而蛋白回收率呈现缓慢上升的趋势,在16 h时达到最高水平(60.85%±2.22%)。
由图2(B)可知,同一酶解时间下,酶解液浓度与ADH激活率呈现正相关趋势。随着时间的延长,1和2.5 mg/mL浓度下酶解液ADH激活率呈现缓慢上升趋势,当酶解时间为12 h时,酶解产物蛋白浓度为2.5 mg/mL 时,ADH激活率为154.01%±2.86%。在酶解液浓度达到5 mg/mL时,ADH激活率呈现先增高后降低的趋势且酶解时间为8 h的ADH激活率最优(175.79%±0.79%)。
图2(C)ABTS+自由基清除能力也呈现出动态变化趋势,这更是说明了不同酶解时间下,动态的多肽释放和序列改变对其活性的影响。其中酶解时间为4 h时ABTS+自由基清除率(38.97%±0.62%)显著高于其他酶解时间(P<0.05)。综合水解度、蛋白回收率、ADH激活率、抗氧化指标以及时间成本,选择8 h酶解时间进行接下来的实验。
2.3 不同酶添加量对鲟鱼子酶解效率及酶解液活性的影响
有研究表明,酶解时间和酶添加量对生物活性多肽的释放具有至关重要的影响[24]。因此,本研究考察了不同复配酶添加量对鲟鱼子酶解效率及酶解液活性的影响。
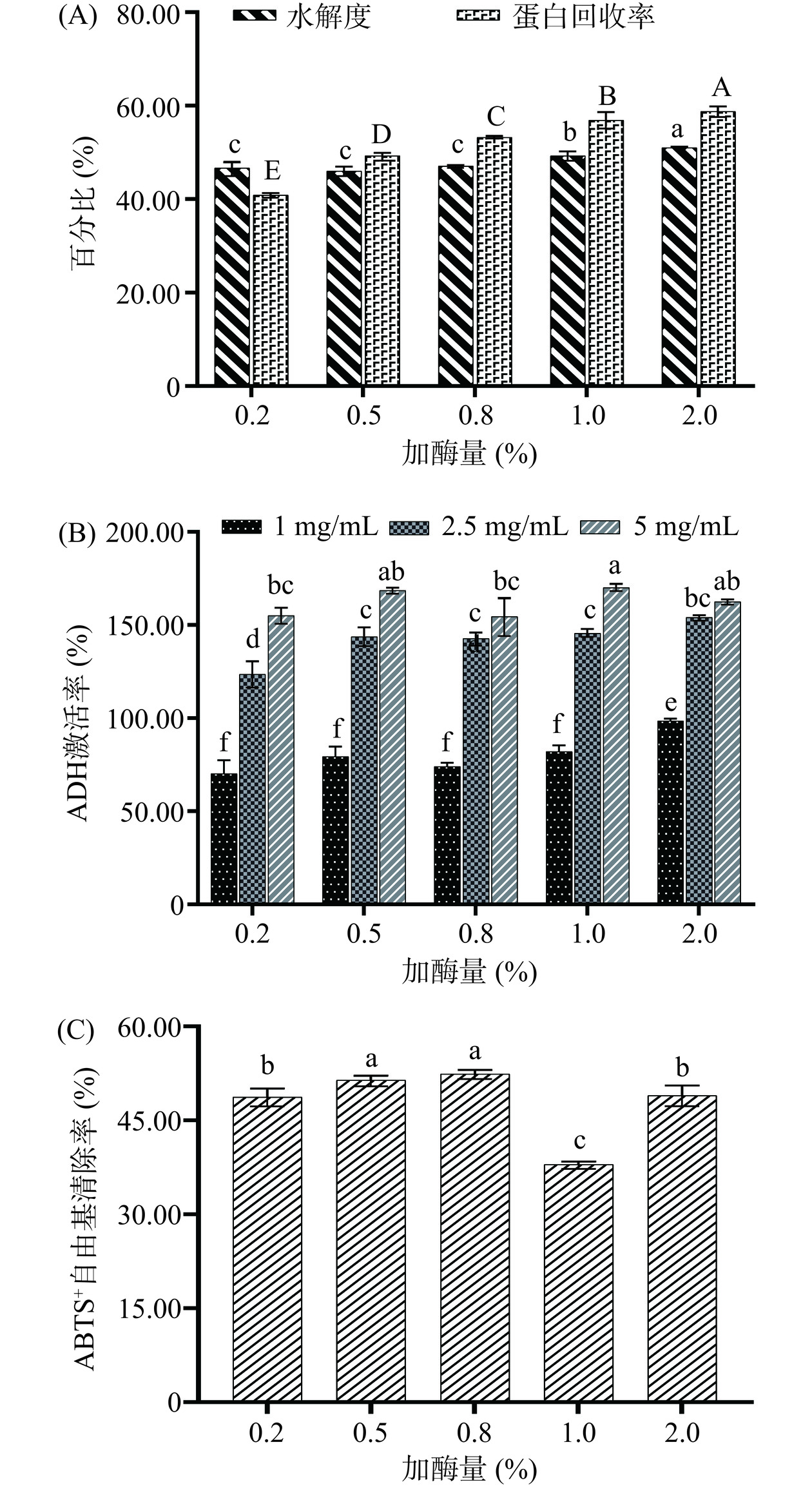
由图3(A)可知,随着添加量的增加,水解度和蛋白回收率均呈现缓慢升高的趋势。其中酶添加量为2%(胰酶108 U+碱性蛋白酶5372 U)时蛋白回收率(58.77%±1.09%)与水解度(51.06%±0.20%)显著高于其他组(P<0.05),这说明酶添加量的增加有助于酶解效率的提升。
由图3(B)可知,同一酶添加量情况下,酶解液浓度与ADH激活率呈正相关;随着酶添加量的增加,不同浓度酶解液ADH激活率呈现缓慢增加的趋势。在鲟鱼子酶解产物浓度为1 mg/mL时,加酶量为2%时与其他组存在显著性差异(P<0.05);在鲟鱼子酶解产物浓度为2.5 mg/mL时,加酶量为0.5%、0.8%、1.0%无显著性差异(P>0.05);在鲟鱼子酶解产物浓度为5 mg/mL时,加酶量为0.5%时与其他组无显著性差异(P>0.05)。
图3(C)ABTS+自由基清除能力则呈现先增加后降低再增加的动态变化趋势。在加酶量为0.5%(51.45%±0.66%)和0.8%时,无显著性差异(P>0.05),因此结合各指标结果与制备成本综合选择0.5%为最佳加酶量。
综合上述因素结合制备成本,选择添加复配酶0.5%(胰酶27 U+碱性蛋白酶1343 U)酶解时间8 h,进行样品制备并研究其对酒精损伤肝细胞的保护作用。在此条件下得到的酶解产物蛋白回收率为49.30%±0.57%,水解度为46.05%±0.92%,自由基清除率为51.45%±0.66%,在1~5 mg/mL时,ADH激活率在79.38%±5.33%~168.64%±1.42%之间。
2.4 鲟鱼子酶解产物对酒精损伤HepG2细胞相对活力的影响
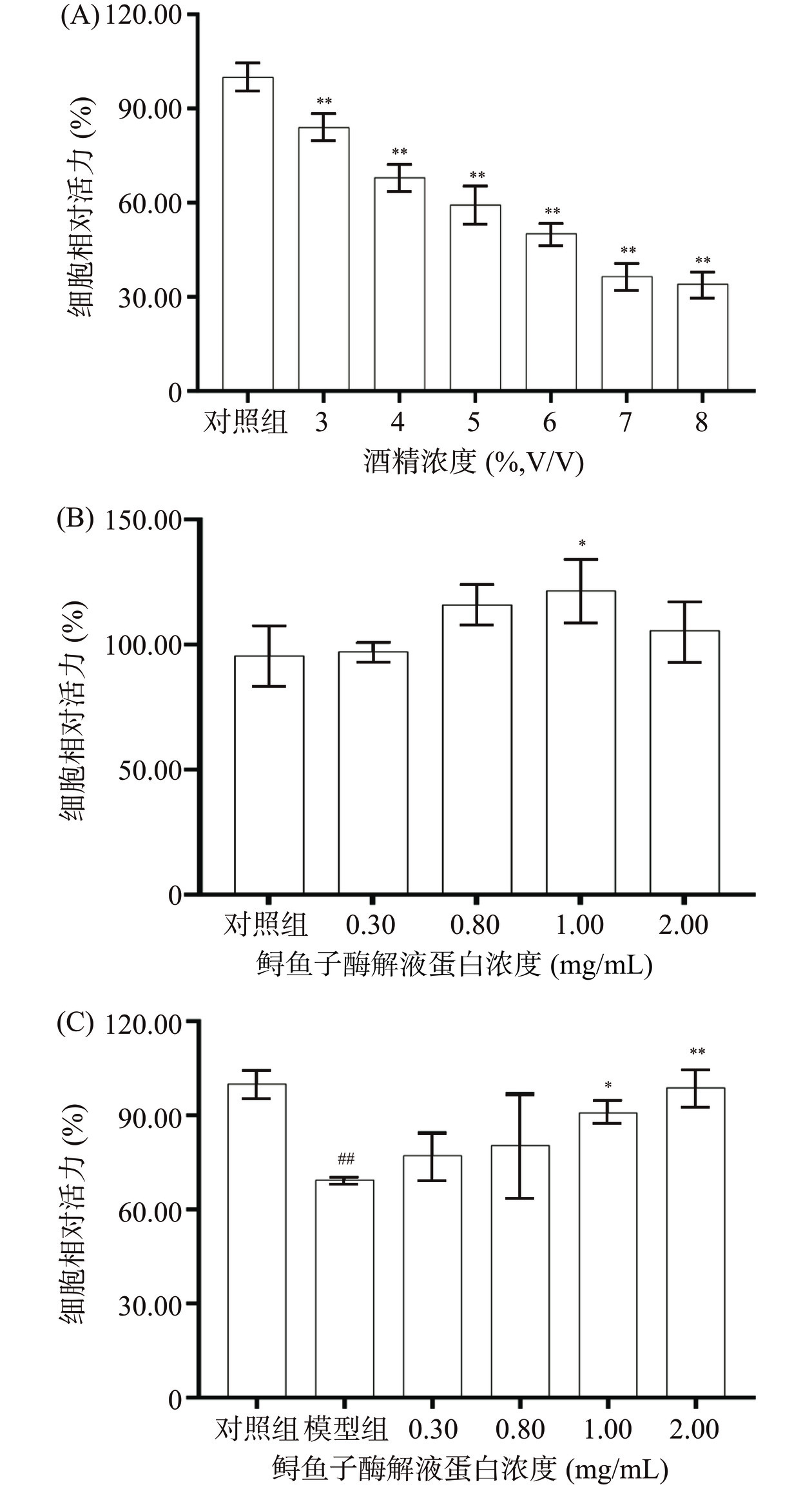
本研究采用酒精损伤HepG2细胞模拟酒精损伤肝细胞状态[25],并研究鲟鱼子酶解产物对其损伤的保护作用。如图4(A)所示,HepG2细胞相对活力随酒精浓度的增加而极显著降低(P<0.01)。当酒精浓度为6%时,HepG2细胞相对活力在50%左右,在此浓度下的酒精给细胞造成损伤但又不至于造成细胞不可逆转的损伤,基于此,本研究选择6%酒精浓度作为建模条件。如图4(B)所示,不同浓度的样品处理组均能提高细胞相对活力,且未观察到样品所致的毒性,当样品浓度为1 mg/mL时能显著升高细胞相对活力(P<0.05)。图4(C)结果显示与对照组相比,模型组细胞相对活力(69.49%±0.90%)极显著下降(P<0.01),表示造模成功。而不同鲟鱼子酶解产物处理组均可提升细胞相对活力,其中1 mg/mL(90.89%±3.98%)与2 mg/mL(98.86%±5.65%)样品处理组细胞相对活力显著提升(P<0.05,P<0.01)。
![]() 图 4 酒精损伤HepG2细胞造模浓度筛选(A)、样品毒性检测(B)和鲟鱼子酶解样品对酒精损伤HepG2细胞的相对活力的影响(C)注:A、B图中,*表示与对照组有显著性差异,P<0.05,**代表与对照组有极显著性差异,P<0.01;C图中,#表示模型组与对照组有显著性差异,P<0.05,##代表模型组与对照组有极显著性差异,P<0.01;*表示处理组与模型组有显著性差异,P<0.05,**代表处理组与模型组有极显著性差异,P<0.01;图5同。Figure 4. Alcohol model concentration screening of alcohol-damaged HepG2 cells (A), sample toxicity (B) and effect of sturgeon roe hydrolyzed samples on the relative viability of alcohol injured HepG2 cells (C)
图 4 酒精损伤HepG2细胞造模浓度筛选(A)、样品毒性检测(B)和鲟鱼子酶解样品对酒精损伤HepG2细胞的相对活力的影响(C)注:A、B图中,*表示与对照组有显著性差异,P<0.05,**代表与对照组有极显著性差异,P<0.01;C图中,#表示模型组与对照组有显著性差异,P<0.05,##代表模型组与对照组有极显著性差异,P<0.01;*表示处理组与模型组有显著性差异,P<0.05,**代表处理组与模型组有极显著性差异,P<0.01;图5同。Figure 4. Alcohol model concentration screening of alcohol-damaged HepG2 cells (A), sample toxicity (B) and effect of sturgeon roe hydrolyzed samples on the relative viability of alcohol injured HepG2 cells (C)2.5 鲟鱼子酶解产物对酒精损伤HepG2细胞生化指标的影响
本研究继续评估了酒精损伤肝细胞的氧化应激和酒精代谢相关指标的变化情况。SOD能消除生物体在新陈代谢过程中产生的有害物质,是细胞内抵抗氧化应激的主要酶系之一[26]。如图5(A)所示,与对照组相比,模型组的SOD酶活性极显著降低(P<0.01),说明细胞的抗氧化机制已被破坏,呈现氧化损伤状态。各样品处理组与模型组比较,SOD酶活性均呈现不同程度的上升,这表明酶解产物处理可以中和酒精引起的氧化应激伤害,并通过增强SOD酶活性来恢复HepG2细胞的抗氧化状态。
作为抗氧化体系中的重要成员,GSH含量的变化能够反映体系的抗氧化能力[27]。由图5(B)所示,与对照组相比,酒精模型组GSH含量极显著降低(P<0.01),不同浓度鲟鱼子酶解液处理组均能极显著地升高GSH含量(P<0.01),由此可见鲟鱼子酶解上清液能促进GSH再生,增强肝脏自由基的清除能力,从而减少由于体内过氧化产物堆积造成对肝脏的损伤,保护肝脏功能。
氧化应激状态下自由基水平的增加会导致脂质过氧化产物丙二醛(MDA)的生成[28]。由图5(C)所示,与对照组相比,酒精模型组MDA水平极显著增加(P<0.01),表示6%酒精能够诱导细胞发生严重的脂质过氧化,与酒精模型组相比,不同浓度鲟鱼子酶解液处理组均能显著减少损伤细胞中MDA含量(P<0.05或P<0.01)。
在MDA和GSH中,样品组在2 mg/mL时出现了高浓度相对抑制效果,这与此前Zhao等[29]的研究结果一致,可能是因为一些多肽对药效的影响呈U型剂量反应,称为双向剂量反应。此外Chen等[30]研究也发现,罗非鱼皮明胶水解物中的YGDEY可以通过调节氧化应激通路实现对HepG2细胞酒精诱导损伤的预防作用。
当肝细胞受到乙醇的伤害时会发生浑浊肿胀,从而增加细胞膜的通透性,并释放AST和ALT。因此,AST和ALT常被用作敏感指标来评估肝损伤[31]。由图5(D)、5(E)可知,与对照组相比,模型组AST和ALT水平极显著升高(P<0.01),而不同浓度的鲟鱼子酶解产物均可显著降低酒精损伤HepG2细胞中的AST和ALT水平(P<0.05或P<0.01)。由此可见,鲟鱼子酶解产物通过降低酒精性损伤引起的ALT和AST活性增加进而起到保护肝细胞的作用。
2.6 鲟鱼子酶解产物中活性肽鉴定与虚拟筛选
Peptide Ranker和CPPpred两种评分工具的分数范围均为0~1,其中分数越高,预示肽段的相关潜力越大。因此本实验将Peptide Ranker、相对峰面积、CPPpred预测等评分指标按从高到低排名,筛选出同时符合Peptide Ranker评分>0.5,CPPpred评分>0.2以及相对峰面积>0.2%条件的肽段,共得到5条具有潜在生物活性的多肽,由图6和表1可知,多肽序列LPG的Peptide Ranker评分最高,为0.97;FLPR的CPPpred评分最高,为0.43;ALPLDPK的相对峰面积最大为0.47%。由表1可知,5个肽的疏水性在+6.89~+12.62 kcal/mol之间,等电点在5.58~10.73之间,净电荷在0~+1之间,相对分子量在285.17~752.44 Da之间。结果表明,鲟鱼鱼子保护肝细胞免受酒精损伤可能与上述5条具有生物活性的肽段有关,需要进一步的实验验证。
表 1 5条肽段的生物学信息Table 1. Biological information of 5 peptides肽序列 相对峰面积(%) CPPpred Peptide Ranker 相对分子质量(Da) 疏水性(kcal/mol) 等电点 净电荷 ALPLDPK 0.47 0.35 0.56 752.44 +12.62 6.44 0 LGGL 0.31 0.37 0.71 358.22 +7.70 5.58 0 KYPL 0.28 0.33 0.59 519.31 +8.88 9.78 +1 LPG 0.22 0.24 0.97 285.17 +7.94 5.58 0 FLPR 0.21 0.43 0.93 531.32 +6.89 10.73 +1 3. 结论
本研究以高蛋白高脂质高水分含量的鲟鱼鱼子为研究对象,通过采用单因素实验,结合酶解效率和酶解产物活性等指标,筛选得到具有较高ADH激活率和抗氧化能力的鲟鱼子复合酶酶解产物。在筛选出的最优酶解条件下蛋白回收率为49.30%±0.57%,水解度为46.05%±0.92%,ABTS+自由基清除率为51.45%±0.66%。进一步利用酒精损伤HepG2肝细胞模型评价其对肝细胞的保护作用,其中1 mg/mL(90.89%±3.98%)与2 mg/mL(98.86%±5.65%)样品处理组细胞相对活力显著提升(P<0.05,P<0.01)。再通过检测GSH、SOD、MDA氧化应激以及AST和ALT活力指标,表明酶解产物能显著改善酒精诱导的肝细胞损伤。继而,本研究利用质谱技术结合虚拟筛选手段,从鲟鱼子酶解产物中得到5条潜在解酒护肝功效的生物活性多肽,为下一步的机制研究奠定了基础。本研究初步证明鲟鱼子酶解产物能够通过改善氧化应激通路,调节酒精代谢等实现对酒精损伤肝细胞的保护作用。
-
图 4 酒精损伤HepG2细胞造模浓度筛选(A)、样品毒性检测(B)和鲟鱼子酶解样品对酒精损伤HepG2细胞的相对活力的影响(C)
注:A、B图中,*表示与对照组有显著性差异,P<0.05,**代表与对照组有极显著性差异,P<0.01;C图中,#表示模型组与对照组有显著性差异,P<0.05,##代表模型组与对照组有极显著性差异,P<0.01;*表示处理组与模型组有显著性差异,P<0.05,**代表处理组与模型组有极显著性差异,P<0.01;图5同。
Figure 4. Alcohol model concentration screening of alcohol-damaged HepG2 cells (A), sample toxicity (B) and effect of sturgeon roe hydrolyzed samples on the relative viability of alcohol injured HepG2 cells (C)
表 1 5条肽段的生物学信息
Table 1 Biological information of 5 peptides
肽序列 相对峰面积(%) CPPpred Peptide Ranker 相对分子质量(Da) 疏水性(kcal/mol) 等电点 净电荷 ALPLDPK 0.47 0.35 0.56 752.44 +12.62 6.44 0 LGGL 0.31 0.37 0.71 358.22 +7.70 5.58 0 KYPL 0.28 0.33 0.59 519.31 +8.88 9.78 +1 LPG 0.22 0.24 0.97 285.17 +7.94 5.58 0 FLPR 0.21 0.43 0.93 531.32 +6.89 10.73 +1 -
[1] 李沛洋, 朱学芝, 李昭林, 等. 鲟鱼营养研究进展[J]. 广东饲料,2021,30(8):33−38. [LI P Y, ZHU X Z, LI Z L, et al. Progress in sturgeon nutrition[J]. Guangdong Feed,2021,30(8):33−38.] doi: 10.3969/j.issn.1005-8613.2021.08.010 LI P Y, ZHU X Z, LI Z L, et al. Progress in sturgeon nutrition[J]. Guangdong Feed, 2021, 30(8): 33−38. doi: 10.3969/j.issn.1005-8613.2021.08.010
[2] FARAG M A, ABIB B, TAWFIK S, et al. Caviar and fish roe substitutes:Current status of their nutritive value, bio-chemical diversity, authenticity and quality control methods with future perspectives[J]. Trends in Food Science & Technology,2021,110:405−417.
[3] TAVAKOLI S, LUO Y, REGENSTEIN J M, et al. Sturgeon, caviar, and caviar substitutes:From production, gastronomy, nutrition, and quality change to trade and commercial mimicry[J]. Reviews in Fisheries Science and Aquaculture,2021,29(4):753−768. doi: 10.1080/23308249.2021.1873244
[4] USMAN M, SAMEEN A, KHAN M I, et al. Introduction to world production of fish roe and processing[M]. Fish Roe:Elsevier, 2022:1–18.
[5] HWANG B B, CHANG M H, LEE J H, et al. The edible insect gryllus bimaculatus protects against gut-derived inflammatory responses and liver damage in mice after acute alcohol exposure[J]. Nutrients,2019,11(4):857. doi: 10.3390/nu11040857
[6] ZHENG J, TIAN X, ZHANG W, et al. Protective effects of fucoxanthin against alcoholic liver injury by activation of Nrf2-mediated antioxidant defense and inhibition of TLR4-mediated inflammation[J]. Marine Drugs,2019,17(10):552. doi: 10.3390/md17100552
[7] YANG Y M, CHO Y E, HWANG S. Crosstalk between oxidative stress and inflammatory liver injury in the pathogenesis of alcoholic liver disease[J]. International Journal of Molecular Sciences,2022,23(2):774. doi: 10.3390/ijms23020774
[8] WANG S, ZHAO M, FAN H, et al. Emerging proteins as precursors of bioactive peptides/hydrolysates with health benefits[J]. Current Opinion in Food Science,2022,48:100914. doi: 10.1016/j.cofs.2022.100914
[9] ETEMADIAN Y, GHAEMI V, SHAVIKLO A R, et al. Development of animal/plant-based protein hydrolysate and its application in food, feed and nutraceutical industries:State of the art[J]. Journal of Cleaner Production,2021,278:123219. doi: 10.1016/j.jclepro.2020.123219
[10] WANG K, SHI J, GAO S, et al. Oyster protein hydrolysates alleviated chronic alcohol-induced liver injury in mice by regulating hepatic lipid metabolism and inflammation response[J]. Food Research International,2022,160:111647. doi: 10.1016/j.foodres.2022.111647
[11] CONTRERAS-ZENTELLA M L, VILLALOBOS-GARCÍA D, HERNÁNDEZ-MUÑOZ R. Ethanol metabolism in the liver, the induction of oxidant stress, and the antioxidant defense system[J]. Antioxidants,2022,11(7):1258. doi: 10.3390/antiox11071258
[12] JIANG Y, ZHANG T, KUSUMANCHI P, et al. Alcohol metabolizing enzymes, microsomal ethanol oxidizing system, cytochrome P450 2E1, catalase, and aldehyde dehydrogenase in alcohol-associated liver disease[J]. Biomedicines,2020,8(3):50. doi: 10.3390/biomedicines8030050
[13] XIAO C, TOLDRÁ F, ZHOU F, et al. Effect of cooking andin vitro digestion on the peptide profile of chicken breast muscle and antioxidant and alcohol dehydrogenase stabilization activity[J]. Food Research International,2020,136:109459. doi: 10.1016/j.foodres.2020.109459
[14] CHEN M F, ZHANG Y Y, DI H M, et al. Antioxidant peptide purified from enzymatic hydrolysates of Isochrysis zhanjiangensis and its protective effect against ethanol induced oxidative stress of HepG2 cells[J]. Biotechnology and Bioprocess Engineering,2019,24:308−317. doi: 10.1007/s12257-018-0391-5
[15] CHO H R, LEE S O. Novel hepatoprotective peptides derived from protein hydrolysates of mealworm (Tenebrio molitor)[J]. Food Research International,2020,133:109194. doi: 10.1016/j.foodres.2020.109194
[16] XIAO C, TOLDRÁ F, ZHOU F, et al. Chicken-derived tripeptide KPC (Lys-Pro-Cys) stabilizes alcohol dehydrogenase (ADH) through peptide-enzyme interaction[J]. LWT,2022,161:113376. doi: 10.1016/j.lwt.2022.113376
[17] ZHAO T, HUANG L, LUO D, et al. Fabrication and characterization of anchovy protein hydrolysates-polyphenol conjugates with stabilizing effects on fish oil emulsion[J]. Food Chemistry,2021,351(5):129324.
[18] SAMAEI S P, GHORBANI M, TAGLIAZUCCHI D, et al. Functional, nutritional, antioxidant, sensory properties and comparative peptidomic profile of faba bean (Vicia faba L.) seed protein hydrolysates and fortified apple juice[J]. Food Chemistry,2020,330:127120. doi: 10.1016/j.foodchem.2020.127120
[19] GONZALEZ-RODRIGUEZ M C, GONZALO C, SAN PRIMITIVO F, et al. Relationship between somatic cell count and lntramammary infection of the half udder in dairy ewes[J]. Journal of Dairy Science,1995,78(12):2753−2759. doi: 10.3168/jds.S0022-0302(95)76906-5
[20] TACIAS-PASCACIO V G, MORELLON-STERLING R, SIAR E H, et al. Use of alcalase in the production of bioactive peptides:A review[J]. International Journal of Biological Macromolecules,2020,165:2143−2196. doi: 10.1016/j.ijbiomac.2020.10.060
[21] MORA L, TOLDRÁ F. Advanced enzymatic hydrolysis of food proteins for the production of bioactive peptides[J]. Current Opinion in Food Science,2022,49:100973.
[22] ZAN R, ZHU L, WU G, et al. Identification of novel peptides with alcohol dehydrogenase (ADH) activating ability in chickpea protein hydrolysates[J]. Foods,2023,12(8):1574. doi: 10.3390/foods12081574
[23] ZHAO T, ZHENG L, ZHANG Q, et al. Stability towards the gastrointestinal simulated digestion and bioactivity of PAYCS and its digestive product PAY with cognitive improving properties[J]. Food and Function,2019,10(5):2439−2449. doi: 10.1039/C8FO02314J
[24] WU S, WANG X, QI W, et al. Bioactive protein/peptides of flaxseed:A review[J]. Trends in Food Science & Technology,2019,92:184−193.
[25] LEE S, LEE J, LEE H, et al. Relative protective activities of quercetin, quercetin-3-glucoside, and rutin in alcohol-induced liver injury[J]. Journal of Food Biochemistry,2019,43(11):e13002.
[26] ALI S S, AHSAN H, ZIA M K, et al. Understanding oxidants and antioxidants:Classical team with new players[J]. Journal of Food Biochemistry,2020,44(3):e13145.
[27] EROL N, SAGLAM L, SAGLAM Y S, et al. The protection potential of antioxidant vitamins against acute respiratory distress syndrome:A rat trial[J]. Inflammation,2019,42:1585−1594. doi: 10.1007/s10753-019-01020-2
[28] ALIZADEH M, KHEIROURI S. Curcumin reduces malondialdehyde and improves antioxidants in humans with diseased conditions:A comprehensive meta-analysis of randomized controlled trials[J]. BioMedicine,2019,9(4):23. doi: 10.1051/bmdcn/2019090423
[29] ZHAO T, ZHONG S, XU J, et al. PAYCS alleviates scopolamine-induced memory deficits in mice by reducing oxidative and inflammatory stress and modulation of gut microbiota-fecal metabolites-brain neurotransmitter axis[J]. J Agric Food Chem,2022,70(9):2864−2875. doi: 10.1021/acs.jafc.1c06726
[30] CHEN M F, GONG F, ZHANG Y Y, et al. Preventive effect of YGDEY from tilapia fish skin gelatin hydrolysates against alcohol-induced damage in HepG2 cells through ROS-mediated signaling pathways[J]. Nutrients,2019,11(2):392. doi: 10.3390/nu11020392
[31] YANG K, ZHAN L, LU T, et al. Dendrobium officinale polysaccharides protected against ethanol-induced acute liver injury in vivo and in vitro via the TLR4/NF-κB signaling pathway[J]. Cytokine,2020,130:155058. doi: 10.1016/j.cyto.2020.155058





 下载:
下载:


 下载:
下载:



